Циклические сульфид
Cтраница 2
 |
Влияние степени конверсии на. [16] |
Реакции циклических сульфидов с металлорганическими соединениями изучены очено мало. [17]
Распределение циклических сульфидов по молекулярным массам устанавливается по ин-тенсивностям пиков молекулярных ионов в тех случаях, когда они достаточно четко отделены от псевдомолекулярных ионов, образующих второй максимум на кривой распределения интенсивностей пиков этого гомологического ряда ионов в области более низких масс. Предварительно должно быть учтено изотопное наложение на основании данных о естественной распространенности изотопов. [18]
Комплексы алифатических и 2-замещенных циклических сульфидов значительно лучше растворяются в ароматических углеводородах, спиртах, чем комплексы 3-замещенных циклических сульфидов. Это свойство было использовано для разделения изомеров сульфидов, что представляет интерес при изучении индивидуального состава нефтяных сульфидов и в процессе синтеза их моделей при разделении изомеров. [19]
Известны также циклические сульфиды, например, этиленсуль-фид А ( темп. [20]
За исключением циклических сульфидов, среди которых наиболее токсичен первый член ряда - этиленсульфид, наиболее токсичные соединения содержат 6 - 8 атомов углерода. Видимо, дальнейшее увеличение числа атомов углерода не ведет к росту токсичности по причинам, о которых говорилось выше, либо структуры, имеющие С8, более ядовиты в силу особых причин. [21]
Характер окисления циклических сульфидов - тиофанов - - мало отличается от окисления алкилсульфидов. Все соединения этого ряда ( за исключением тиофана) весьма трудно доступны. Они подвергались окислению только с целью идентификации, поэтому выходы продуктов окисления, за редким исключением, в литературе не приводятся. [22]
Особым типом циклических сульфидов являются тиираны как из-за особенностей метода их синтеза, так и по причинам своеобразия их реакций. [23]
В спектрах циклических сульфидов положение длинноволновой полосы зависит от размеров полимети-ленового кольца: в триметиленсульфиде она лежит при 275 нм, в тетраметиленсульфиде - при 240 нм и только в пентаметилен-сульфиде достигает 229 нм, как в алифатических сульфидах. Коротковолновая полоса сохраняет свое положение. [24]
Для размыкания циклических сульфидов с целью получения сульфо-кислот приходится применять относительно сильные окислители. Псевдотиогидантоин в разбавленной соляной кислоте ( уд. [25]
Каталитическое дегидрирование циклических сульфидов в тиофены. [26]
 |
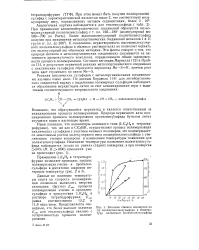
Зависимость lg а от величин, обратных абсолютной температуре, для превращения 2-к-гексилтиофана. [27] |
При превращении циклических сульфидов над шариковым алюмосиликатным катализатором имеет место внутридиффузионное торможение. [28]
Спектры поглощения циклических сульфидов мало отличаются от спектров поглощения диалкилсульфидов. Заметное поглощение в спектрах этих соединений ( lg e 1) начинается около 260 ммк, перегиб наблюдается в области 235 ммк. [29]
Одним из циклических сульфидов - тиациклопентан ( тетрагидротиофен) [10] - был изучен отдельно. Так как термическое разложение этого соединения сопровождается частичной дегидрогенизацией ( до тиацикло-пентена и тиофена), механизм реакции усложняется присутствием водорода, что сообщает этому процессу характер деструктивной дегидрогенизации. Сернистые продукты в этих опытах были представлены, главным образом, сероводородом и тиофеном и в небольших количествах меркаптанами. [30]
Страницы: 1 2 3 4