Внешняя координационная сфера
Cтраница 2
В настоящем обзоре делается попытка оценить влияние природы катиона и аниона, находящегося во внешней координационной сфере комплекса, на силовую постоянную О - Н - связи координированных молекул воды. [16]
Растворяясь в воде, комплексные электролиты диссоциируют на комплексные ионы и ионы, входящие во внешнюю координационную сферу. [17]
 |
Координационные числа ионов металлов ( комплексообразователей. [18] |
Остальные ионы, окружающие комплекс, находятся на более далеком расстоянии от центрального иона и составляют внешнюю координационную сферу. При написании формулы для разделения сфер внутренняя сфера вместе с комплексообразовате-лем заключается в квадратные скобки. [19]
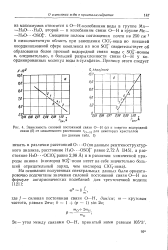 |
Зависимость силовой постоянной связи О - Н ( о и энергии водородной связи ( б от межатомного расстояния о-н для некоторых кристаллов ( по данным 1. [20] |
Смещение полосы поглощения почти на 250 см в низкочастотную область при замещении СЮ - иона во внешней координационной сфере комплекса на ион SOl - свидетельствует об образовании более прочной водородной связи воды с ЗО - ионом и, следовательно, о большей разрыхленности связи О - Н у координированных молекул воды в сульфатах. [21]
Остальные ионы, не разместившиеся во внутренней сфере, находятся на более далеком расстоянии от центрального иона, составляя внешнюю координационную сферу. Число лигандов, окружающих центральный ион, называется координационным числом. [22]
 |
Структура пятихлори - залось также средством наблюде-стого фосфора. н-ия за изменением внутреннего. [23] |
Изучение строения большого числа комплексных соединений показало, что быстрый обмен обычно претерпевают атомы и группы, находящиеся во внешней координационной сфере, в то время как атомы и групиы внутренней сферы обмениваются медленно или вообще не обмениваются. [24]
Получив в синтезах а и б два изомера, можно определить, как различается в них количество хлора, находящегося во внешней координационной сфере. [25]
Первое слагаемое в скобках отражает кулоновское взаимодействие заряженных частиц - участников обмена, второе - изменение энергии, связанное с перегруппировкой растворителя во внешней координационной сфере. На основе расчетов по уравне-ниям ( 1.11) и (1.12) удалось показать удовлетворительное согласие экспериментальных и вычисленных значений / d - ом и A WI-OM для некоторых неорганических и органических редокс-систем. [26]
Огромное разнообразие тетрацидо-соединений обусловлено возможностью варьирования природы центрального атома Me и кислотных остатков X, не говоря уже о варьировании радикалов, находящихся во внешней координационной сфере. [27]
Данные об изменении частот, силовых констант и межатомных расстояний указывают на существенное смещение заряда катиона и деформацию водородных связей, соединяющих молекулы воды во внешней координационной сфере. [28]
Согласно определению Бека [48], в понятие внешнесферных комплексов входит взаимодействие координационно-насыщенных комплексных ионов с другими лигандами, вследствие чего эти лиганды определенным образом удерживаются во внешней координационной сфере комплексо-образователя. [29]
Для комплексов диссоциация протекает в незначительной степени, зависящей от энергии и полярности донорно-акцепторной связи между комплексообразователем и лигандом в то время, как ионы, составляющие внешнюю координационную сферу комплексного соединения, в растворе существуют самостоятельно. [30]
Страницы: 1 2 3 4