7-изомер
Cтраница 1
Токсичность 7-изомера гексахлорциклогексана изменяется в зависимости от температуры внешней среды. При понижении температуры воздуха усиливается его контактное и кишечное действие, а с повышением температуры усиливается фумигационное действие, но прк этом сокращается продолжительность действия. [1]
Для определения содержания 7-изомера в продажном неочищенном гексахлоране - Cl36 применяют метод, основанный на разбавлении анализируемой навески химически чистым - j - изо-мером обычного изотопного состава. Из смеси, которая образуется после добавления определенного количества обычного f - изомера, экстрагируют чистый - изомер - С. [2]
Низкая температура плавления 7-изомера в сравнении с температурой плавления других изомеров использована в японском патенте213 для получения обогащенного продукта. Сущность процесса по этому патенту сводится к следующему. [3]
Основным действующим началом является 7-изомер гекса-хлорциклогексана, остальные изомеры-малотоксичны. [4]
Соотношение 6 - и 7-изомеров, вероятно, определяется пространственными затруднениями на заключительном этапе образования гетероцикла. Как правило, при реакции Неницеску продукты образуются с низкими выходами. [5]
Столь же легко изомеризуются в 1 7-изомеры ne u - дигало-геннафталины. [6]
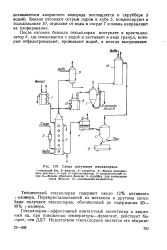 |
Схема получения гексахлорана. [7] |
Технический гексахлоран содержит около 12 % активного 7-изомера. Перекристаллизацией из метанола и другими способами получают гексахлоран, обогащенный до содержания 20 - 99 % i-изомера. [8]
В случае если на переработку поступает высокообогащенный гексахлоран или 7-изомер, достаточна добавка активированного угля в количестве, не превышающем 1 - 2 % по отношению ко взятому гексахлорану. [9]
Серный ангидрид дает примерно в 2 раза больший выход 7-изомера по сравнению с любым из трех других испытанных реагентов. Бензоидное ядро, как и следовало ожидать, сульфируется значительно легче, чем ядро, содержащее атом азота. Комплекс S03 - пиридин не сульфирует азантрахинон вследствие малой реакционной способности как реагента, так и самого соединения. [10]
При нагревании до 450 С 1 2-изомер перегруппировывается в 1 7-изомер. [11]
Взаимодействие D-глкжозы с ( С) приводит к образованию преимущественно 7-изомера [174, 175], а при проведении реакции в присутствии гидразина получается два изомера, причем 6-замещенный птерин получается в большем количестве, чем его 7-изомер. Этот факт указывает на то, что в процессе реакции под влиянием гидразина происходит изомеризация альдоз в кетозы, в результате чего последние образуют с ( С) 6-полиокси-алкилптерины. [12]
Дериваты 2 6-диметилнафталина дегидрируются труднее, чем соответствующие производные 2 7-изомера и, хотя оба ряда веществ обладают смачивающим действием, - повидимому первый ряд в этом отношении значительно превосходит второй. [13]
Приведенный выше механизм необратимой изомеризации 1 8-дизамещенных производных нафталина в 1 7-изомеры подразумевает внутримолекулярное перемещение мигрирующего заместителя. По иному механизму протекает описанное Армстронгом и Уинном [1] превращение 1 8-дихлорнафталина в 1 5-изомер. [14]
Метилптеридины должны быть гораздо более реакционноспособ-ными, чем 6 - и 7-изомеры. [15]
Страницы: 1 2 3 4