Температура - замерзание - чистый растворитель
Cтраница 1
 |
Понижение температуры замерзания раствора. Г0 - температура замерзания растворителя. TI - раствора. [1] |
Температура замерзания чистого растворителя определяется равенством давления его пара над твердой и жидкой фазами. [2]
Температуру замерзания чистого растворителя измеряют несколько раз. [3]
Определив температуры замерзания чистого растворителя и раствора, вычислить понижение-температуры замерзания раствора и, подставив значение At в уравнение Росм 12 04, вычислить величину осмотического давления раствора. [4]
Определяют понижение температуры замерзания чистого растворителя, как описано выше. [5]
 |
Графическое интегрирование прн вычислении коэффициента активности. [6] |
Определяют понижение температуры замерзания чистого растворителя, как описано выше. Измеряют понижение температуры замерзания раствора при 4 - 5 концентрациях, вводя каждый раз в криоскоп примерно 1Д - Vs часть от навески. [7]
Разность между температурами замерзания чистого растворителя и раствора ДГ3 возрастает с повышением концентрации раствора. Как правило, из раствора вначале выкристаллизовывается растворитель. Это способствует дальнейшему понижению температуры замерзания вследствие повышения концентрации раствора. Поэтому замерзание растворов идет в некотором интервале температур. [8]
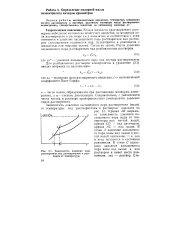 |
Зависимость давления пара растворителя над растворителем и раствором от температуры. [9] |
Задачи работы: экспериментально определить температуру замерзания чистого растворителя и раствора, рассчитать молярную массу растворенного неэлектролита ( лекарственного вещества) по найденному значению ДГ. [10]
Прежде всего необходимо точно определить температуру замерзания чистого растворителя. Для этого взвешивают с точностью-до 0 01 г на технических весах сухой криоскоп ( рис. V. Для этого вставляют термометр в пробку так, чтобы при закрывании криоскопа пробкой нижний резервуар термометра находился на расстоянии 0 5 - 1 см от дна пробирки. Отмечают на криоскопе чертой высоту верхнего уровня ртути в нижнем резервуаре. Вынимают термометр с пробкой и наливают растворитель в криоскоп до метки. Взвешивают криоскоп с растворителем. Опускают в криоскоп мешалку, вставляют термометр Бекмана с пробкой, одевают на криоскоп широкую пробирку и погружают в холодильник. [11]
 |
Экстраполяция значений молекулярной д массы растворенного вещества на нулевое значение концентрации. 0. [12] |
Определив показание термометра, отвечающее температуре замерзания чистого растворителя, приступают к определению молекулярной массы растворенного вещества. Для этого взвешивают на аналитических весах узкую стеклянную пробирку с исследуемым веществом. Затем через тубус криоскопа часть вещества вводят в криоскоп, а пробирку снова взвешивают. По разности масс пробирки до и после введения вещества в криоскоп находят количество вещества. Чем меньше навеска, тем более строго применима формула ( V. [13]
Для разбавленных растворов разница между температурами замерзания чистого растворителя и раствора небольшая. Можно принять, что в этом небольшом температурном интервале теплота плавления растворителя ( точнее - теплота растворения кристаллов в растворе) остается постоянной, и интегрировать уравнение ( IX, Юа) при этом допущении. [14]
Температура замерзания растворов также отличается от температуры замерзания чистых растворителей. Известно, что жидкость замерзает при той температуре, при которой давление пара вещества в твердом состоянии становится равным давлению пара этого же вещества в жидком состоянии. Например, при 0 С давление пара льда ( 613 3 н / Ои2) равно давлению пара воды. Лед и вода могут одновременно сосуществовать друг с другом при температуре, которая носит название температуры замерзания. [15]
Страницы: 1 2 3 4