Температура - замерзание - чистый растворитель
Cтраница 2
Температура замерзания растворов также отличается от температуры замерзания чистых растворителей. [16]
Устанавливается он так, чтобы при температуре замерзания чистого растворителя мениск ртути находился в верхней части шкалы. [17]
Определив отсчет по термометру, отвечающий температуре замерзания чистого растворителя, приступают к определению молекулярного веса растворенного вещества. С этой целью взвешивают на аналитических весах узкую стеклянную пробирку ( трубку) с исследуемым веществом. [18]
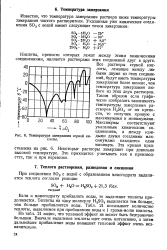 |
Температура замерзания серной кислоты. [19] |
Известно, что температура замерзания раствора ниже температуры замерзания чистого растворителя. [20]
При определении молекулярного веса вещества определяют разность температур замерзания чистого растворителя и раствора. Поступают при этом следующим образом. В сухую и чистую пробирку 3 наливают такое количество чистого растворителя, чтобы ртутный шарик термометра был бы полностью погружен в жидкость. Количество растворителя определяют по разности весов наполненной и пустой пробирки. Взвешивание производят на технических весах с точностью до 0 1 г. Затем в пробирку вставляют пробку с термометром и мешалкой и производят приблизительное определение, показания термометра при замерзании жидкости. Для этого помещают пробирку 3 непосредственно в охлаждающую среду и охлаждают ее лри перемешивании. Момент замерзания определяют по выпадению кристаллов. После этого, осторожно нагревая пробирку, полностью расплавляют кристаллы, стараясь при этом по возможности не перегреть жидкость ( если жидкость все же перегреется, то следует охладить ее до температуры на 0 5 град выше найденной ранее приблизительно температуры замерзания, вновь погрузив пробирку в охлаждающую среду), и производят точное определение показания термометра при замерзании. При этом пробирку 3, вставив ее предварительно в пробирку 2, охлаждают через воздушную прослойку. [21]
Наивысшая температура, при которой приходится работать, равна температуре замерзания чистого растворителя ( для бензола 5 5 С), поскольку растворы будут замерзать при более низкой температуре. Перед началом определения следует установить термометр так, чтобы ртуть при температуре замерзания растворителя ш ходилась в верхней части шкалы - между четвертым и пятым делениями. Если в качестве растворителя применяют бензол, тзрмометр помещают в охлажденную воду, имеющую температуру 5 5 С. Если до этого термометр был установлен для работи на другие температуры, то в нижнем резервуаре может оказаться или больше, чем нужно, или меньше ртути. [22]
Измерение понижения температуры начала замерзания раствора по сравнению с температурой замерзания чистого растворителя называется криоскопией. [23]
Экспериментальная задача криометрии заключается в том, чтобы сначала определить температуру замерзания чистого растворителя - воды, затем ту же величину для двух растворов мочевины различной концентрации. Из полученных данных необходимо вычислить молекулярный вес мочевины. [24]
Изучая растворы, М. В. Ломоносов установил, что температура замерзания раствора ниже температуры замерзания чистого растворителя и что повышение концентрации раствора вызывает понижение температуры его замерзания. [25]
Показать, что температура замерзания раствора нелетучего вещества понижается по сравнению с температурой замерзания чистого растворителя. [26]
Молекулярную массу нефтяных фракций чаще всего устанавливают криоскопическим методом, основанным на определении температуры замерзания чистого растворителя, а затем растворителя с добавлением исследуемого вещества. Растворы замерзают при более низкой температуре, чем чистые растворители; понижение температуры ( депрессия) пропорционально концентрации исследуемого вещества и одинаково для данного растворителя при эквимолекулярных растворах. [27]
При более точных расчетах активностей эту зависимость необходимо учитывать, в особенности если изменение температуры замерзания чистого растворителя А Г велико. [28]
Если работают с летучим растворителем ( например, бензолом), взвешивать лучше после определения температуры замерзания чистого растворителя, непосредственно перед введением растворенного вещества. [29]
Температура кипения растворов нелетучих твердых веществ в жидкостях выше температуры кипения чистого растворителя; температура замерзания ниже температуры замерзания чистого растворителя, что является следствием закона Рауля. [30]
Страницы: 1 2 3 4