Температура - замерзание - чистый растворитель
Cтраница 3
Известно, что растворы, как правило, замерзают при температурах, более низких по сравнению с температурой замерзания чистого растворителя, причем температура замерзания раствора зависит от его концентрации и природы растворителя. [31]
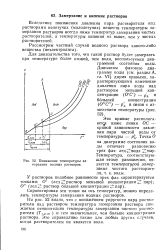 |
Понижение температуры замерзания водных растворов. [32] |
На рис. 52 видно, что с понижением упругости пара растворителя над раствором температура замерзания раствора снижается относительно температуры замерзания чистого растворителя ( Гз. Это справедливо также для любых других случаев, когда растворителем не является вода. [33]
Для получения более верного отсчета рекомендуется не допускать переохлаждения раствора больше чем на 0 5 по сравнению с температурой замерзания чистого растворителя. [34]
Криоскопический метод определения молекулярной массы какого-либо вещества основан на понижении температуры замерзания раствора этого вещества по сравнению с температурой замерзания чистого растворителя. В качестве растворителя легких фракций нефти обычно употребляют бензол, а более высокомолекулярных фракций - нафталин, камфару. [35]
В результате опыта получаем следующие данные: q - вес растворителя, g - вес растворенного вещества, t - температура замерзания чистого растворителя, t2 - температура замерзания раствора. [36]
 |
Прибор для определения молекулярного веса криоскопическим методом. [37] |
В результате опыта получаем следующие данные: q - вес растворителя, g - вес растворенного вещества, t - температура замерзания чистого растворителя, tz - температура замерзания раствора. [38]
Другим весьма важным следствием понижения давления пара раствора нелетучим растворенным веществом является то, что температура замерзания раствора становится ниже температуры замерзания чистого растворителя, которая определяется условием равенства давления его пара над жидкой и твердой фазами. Если при замерзании раствора выделяется чистый растворитель, то давление пара над раствором также должно быть равно давлению растворителя в твердом состоянии. [39]
Здесь К - криоскопическая постоянная растворителя или моляльное понижение температуры замерзания [ К - кмоль / кг ]; Гпл - температура замерзания чистого растворителя, К; / пл - удельная теплота плавления растворителя, Дж / кг. [40]
Определение массы моля вещества с достаточно большой точностью можно получить, применяя растворитель с большой криоскопической константой и значительной разницей между температурой замерзания чистого растворителя и раствора. [41]
Мольное понижение температуры замерзания ( крио-скопическая константа) соответствует понижению температуры раствора, содержащего 1 моль частиц растворенного вещества в 1000 г растворителя, по сравнению с температурой замерзания чистого растворителя. [42]
Таким образом, в рамках принятой модели оказывается, что температура, при которой скорость реакции максимальна, зависит только от энергии активации реакции в жидкой фазе и температуры замерзания чистого растворителя. [43]
 |
Диаграмма, поясняющая связь между понижением давления пара и понижением температуры замерзания. [44] |
Если из раствора кристаллизуется не чистый растворитель, а смешанные кристаллы растворителя и растворенного вещества ( твердый раствор), то температура кристаллизации твердого раствора может быть ниже температуры замерзания чистого растворителя или выше ее. [45]
Страницы: 1 2 3 4