Температура - кристаллизация - вещество
Cтраница 2
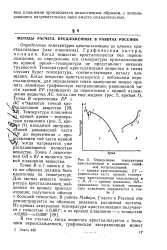
Когда вещество кристаллизуется без переохлаждения, то определение его температуры кристаллизации из кривой время - температура не представляет никаких трудностей. Температурой кристаллизации вещества в таких случаях будет температура, соответствующая началу площадки. Температура плавления из кривой время - температура плавления ( рис. 5, кривая / /) находится экстраполяцией равновесной части GH до пересечения с продолжением той части кривой / С /, когда нагревается уже расплавившееся полностью вещество. Точка / пересечения GH с / С / и является точкой плавления вещества. [16]
Когда вещество кристаллизуется без переохлаждения, то определение его температуры кристаллизации из кривой время-температура не представляет никаких трудностей. Температурой кристаллизации вещества в таких случаях будет температура, соответствующая началу площадки. [18]
Так как температура кристаллизации веществ слабо зависит от давления, то для таких систем пересыщение обычно создается путем охлаждения расплавов. [19]
Многие органические вещества кристаллизуются с большим переохлаждением. Наличие переохлаждения увеличивает возможность ошибки при определении температуры кристаллизации вещества, так как в таких случаях требуется большая экстраполяция, которая при больших переохлаждениях может внести ошибку. [20]
Без разрежения в рубашке сосуда большая разность температур кристаллизации вещества и температуры хладо-агента приводит к очень быстрой кристаллизации, при которой трудно замерить площадку на кривой. [21]
Выбрав подходящие вещества для нужного интервала температур, расплавляют их, как обычно, в тиглях или пробирках и записывают их кривые охлаждения. На кривых охлаждения находят остановки, отвечающие температуре кристаллизации вещества, и строят по ним калибровочную кривую. [22]
Выбрав подходящие вещества для нужного интервала температур, расплавляют их в тиглях или пробирках и записывают их кривые охлаждения. На кривых охлаждения находят остановки, отвечающие температуре кристаллизации вещества, и строят по ним калибровочную кривую. [23]
Выбрав подходящие вещества для нужного интервала температур, расплавляют их, как обычно, в тиглях или пробирках и записывают их кривые охлаждения. На кривых охлаждения находят остановки, отвечающие температуре кристаллизации вещества, и строят по ним калибровочную кривую. [24]
Охладительная игла представляет собой нихромовую проволоку диаметром 1 мм, которая все время находится в жидком азоте и охлаждается до его температуры. Так как охладительная игла имеет температуру значительно более низкую, чем температура кристаллизации вещества, то в момент внесения ее в вещество она вызывает кристаллизацию, образуя участки с более низкой температурой. Эффективность действия усиливается, если иглой потереть о стенку сосуда. [25]
Охладительная игла представляет собою нихромовую проволоку диаметром 1 мм или тонкую стеклянную палочку, которая все время находится в жидком азоте и охлаждается до его температуры. Так как охладительная игла имеет температуру значительно более низкую, чем температура кристаллизации вещества, то в момент внесения ее в вещество она вызывает кристаллизацию, образуя участки с более низкой температурой. Эффективность действия усиливается, если иглой потереть о стенку сосуда. [26]
 |
Сосуд для кристаллизации ( или плавления вещества, применявшийся Майером. [27] |
Вторым экспериментальным требованием при оценке количества примесей из кривых время - температура кристаллизации ( или плавления) является соблюдение постоянной скорости кристаллизации вещества. Для выполнения этого берется хладоагент, имеющий постоянную температуру, которая намного ниже температуры кристаллизации вещества. Величина же скорости охлаждения регулируется переменным вакуумом, создаваемым в рубашке сосуда с исследуемым веществом. [28]
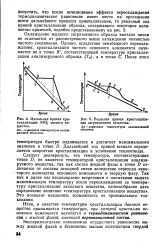 |
Идеальная кривая кристаллизации 100 % чистого вещества.| Реальная кривая кристаллизации загрязненного вещества. RS - изменение температуры охлаждающей. [29] |
Следует подчеркнуть, что температура, соответствующая точке D, не является температурой кристаллизации анализируемого вещества, так как состав жидкой фазы в точке D отличается от состава исходной смеси вследствие перехода некоторого количества основного компонента в твердую фазу. Так как и далее мы неоднократно встретимся с попытками выдать максимальную температуру после переохлаждения за температуру кристаллизации исходного вещества, целесообразно дать определение величине температура кристаллизации вещества. [30]
Страницы: 1 2 3