Температура - начало - взаимодействие
Cтраница 1
Температура начала взаимодействия ура-а с водородом колеблется в пределах от комнатной до 100 С IB зависимости от дислерснвсти урана. UHs образуется при температуре 200 - 3l ( fC, при увеличении температуры разлагается. [1]
Температура начала взаимодействия водорода с торием с образованием гидридов зависит от дисперсности металла и чистоты поверхности. Компактный торий быстро реагирует с водородом при температурах 200 - 300 С, а порошкообразный - при комнатной. [2]
Одним из путей снижения температуры начала взаимодействия является способ повышения химической активности осаждаемого материала за счет введения в частицу окисла структурных фрагментов шпинели Me - О-Me с ослабленными связями. [3]
По данным гравиметрических исследований, температура начала взаимодействия соответствует 1200 С, при этом, однако, не наблюдается появления новых фазовых составляющих в структуре образцов. На рис. 29 показана зависимость степени восстановления SrO от времени при заданных температурах. [4]
Исследование каждой композиции включает определение температуры начала взаимодействия, описания некоторых кинетических закономерностей, а также фазовый анализ продуктов взаимодействия и выяснение, таким образом, наиболее вероятной схемы ( реакции) взаимодействия. Результаты кинетических исследований по каждой системе МегС - МеО, МеЮ - МеО представлены графическими зависимостями. [5]
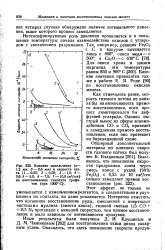 |
Влияние измельчения ( а - 1 2 мм. б - 0 6 мм и скорости азота ( / - 0 25. 2 - 0 50. 3 - 1 0. 4 - 3 0. 5 - 5 0. 5 - 7 5. 7 - 10 0 см3 / сек, на восстановление гематита графитом ( при 1000 Q. [6] |
Интенсифицирующая роль давления проявляется и в повышении температуры начала взаимодействия окислов с углеродом с увеличением разряжения. [7]
Результаты экспериментальных исследований свидетельствовали о том, что температура начала взаимодействия составляет примерно 1300 С. Процесс взаимодействия сопровождается появлением новой ( неидентифицированной) фазы ( Х - фаза), которая сохраняется до 1700 С. [8]
Эти результаты свидетельствуют о том что фиксируемая гравиметрическим методом температура начала взаимодействия при 1300 - 1400 С характеризуется появлением в системе новой фазовой составляющей, идентифицируемой как ЗгТЮз. Указанная фаза без изменения кристаллической структуры сохраняется для состава 50 % TiC 50 % SrO до 1600 С. [9]
В сводных табл. 4 и 5 представлены результаты определения значений температур начала взаимодействия наиболее вероятных реакций при р и 5 - 10 - 7 ат соответственно. [10]
Чем выше степень чистоты материала и его плотность, тем более высоки температуры начала взаимодействия. [11]
Ко второй категории химических процессов мы относим такие, у которых, во-первых, температура начала взаимодействия лежит выше обыкновенной температуры; во-вторых, во время взаимодействия развивается температура высшая, чем температура начала реакции, а потому, раз начавшись и требуя для начала повышения температуры от постороннего тела, реакции этого рода идут затем сами собою, не требуя нагревания, а, напротив того, доставляя его. Несомненно, что для всякого химического изменения имеется такой предел низшей температуры, ниже которого данное химическое явление не совершается со всею его массою и если происходит, то в месте соприкосновения с третьим, посторонним телом, могущим при этом не изменяться. Влия ние прикосновения станет понятным, если узнаем, что на всякой поверхности, ограничивающей тело, движение его частей должно претерпеть особое изменение, могущее быть подобным изменению, совершающемуся при нагревании. Очевидно, что изменение, производимое прикосновением к третьему телу, не касается существа дела о влиянии температуры, хотя и играет свою роль. Так, фосфор на своей поверхности поглощает кислород и при обыкновенной температуре, но для зажигания фосфора нужна температура выше обыкновенной. Так, желтый фосфор при обыкновенной температуре, по крайней мере в темноте, нисколько не превращается в красный фосфор. Правда, что при действии света и при обыкновенной температуре происходит медленное поверхностное изменение желтого фосфора в красный; но это уже другая сторона предмета, которой нам здесь нет нужды касаться и которая имеет свой особый интерес в теоретическом отношении, однако, до сих пор в практике не оказывающем влияния. [12]
Несмотря на неравновесные состояния механически активируемых твердофазных реагентов, термодинамические расчеты используют для оценки температуры начала взаимодействия. [13]
Представленный материал справочника характеризует в заданных условиях для каждой из рассматриваемых систем ( в пределах имеющихся данных) температуру начала взаимодействия компонентов и специфические особенности развивающихся процессов. [14]
Бомбу с шихтой, состоящей из четырехфтористого урана и металлического магния, после откачивания воздуха нагревают в печи до температуры начала взаимодействия компонентов шихты. Вследствие экзотер-мичности реакции и большой скорости ее протекания реакционная смесь плавится и металлический уран вытекает в углубление донной части бомбы, где затвердевает в слиток при охлаждении бомбы. Охлажденный металл после очистки от шлака поступает на плавление и отливку. Металлические отходы и шлак возвращают на очистку вместе с урановым концентратом. [15]
Страницы: 1 2 3