Температура - начало - взаимодействие
Cтраница 3
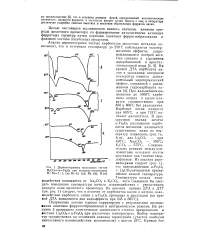 |
Дериватограммы модельных систем M2COs aFe2Oa при мольных отношениях М. Fe 1. 1, где М - Li ( a. Na ( б. К ( в. [31] |
С карбонаты натрия и калия плавятся соответственно пр 830 и 860 С без разложения. Карбонат лития плавится при 685 С, а при 715 С начинает разлагаться. Следовательно, реакции между компонентами исходной шихты протекают как типично твердофазные. Из анализа дери-вакирамм следует ( рис. 1), что взаимодействие а - Рб2Оз с Li2CO3 начинается при наиболее низкой температуре. Температура начала взаимодействия понижается от Na2CO3 к К2СОз, хотя следовало бы ожидать повышения температуры начала взаимодействия с увеличением радиуса иона щелочного промотора. [32]
С карбонаты натрия и калия плавятся соответственно пр 830 и 860 С без разложения. Карбонат лития плавится при 685 С, а при 715 С начинает разлагаться. Следовательно, реакции между компонентами исходной шихты протекают как типично твердофазные. Из анализа дери-вакирамм следует ( рис. 1), что взаимодействие а - Рб2Оз с Li2CO3 начинается при наиболее низкой температуре. Температура начала взаимодействия понижается от Na2CO3 к К2СОз, хотя следовало бы ожидать повышения температуры начала взаимодействия с увеличением радиуса иона щелочного промотора. [33]
Так, например, сода с песком в твердом состоянии совсем не реагируют. Причину этого можно прежде всего искать уже в том, что оба вещества суть тела твердые. Химический же процесс есть образование однородного вещества. Следовательно, он непременно должен состоять в движении частиц, в проникновении одного тела другим, и требует поэтому, чтоб хотя одно из действующих веществ было в подвижно-жидком или газообразном состоянии. Это не исключает, однако, возможности взаимодействия в порош-коватых массах, смешанных и особенно подвергнутых затем сильному сжатию, которое и имеет тот смысл, что при нем поверхности сближаются и в точках прикосновения наступает изменение структуры или состояния движения вещества, могущее быть подобным тому изменению, которое наступает при нагревании. В норме, однако, подвижность жидкого или газового состояния нужна для обычного хода химического изменения. Однако при температуре плавления соды, между песком и содою еще нет взаимодействия, по крайней мере в количествах, сколько-нибудь практически очевидных. Нагревание требуется довести далее до того, чтобы углекислый газ выделился, и из соды и песку получилось бы сплавленное стекло. Нам не нужно здесь входить в рассмотрение того, почему нужна температура известной высоты для известного химического процесса. Важно только знать в каждом частном случае, какая темлература представляет начало взаимодействия, потребного в заводском деле. Но в действительности приходится вести нагревание не только до этой температуры начала взаимодействия, а иногда горазда дальше, - до той температуры, при которой взаимодействие или изменение достигает наибольшей напряженности, чтобы сократить время реагирования. Это последнее ведет и к экономии топлива, потому что продолжительное нагревание, хотя. Следовательно, для сокращения расходов топлива нужно знать в каждом частном случае, какая температура наиболее благоприятна ходу известного превращения. О количестве же расходуемого топлива можно судить, зная уже температуру и другие ей отвечающие ( теплоемкость, массу) элементы, точно того же рода, как при нагревании, что было выше разобрано. [34]
Страницы: 1 2 3