Температура - реагирующая смесь
Cтраница 1
Температура реагирующей смеси может достигнуть 3000 С. [1]
Если температура реагирующей смеси ниже 25, образовавшийся гидросульфит натрия способен соединяться с еще неразложенным гидросульфитом цинка и образовать двойную соль, плохо растворимую в воде. Эта соль при фильтрации остается на фильтре вместе с осадком углекислого цинка и вызывает дополнительные потери гидросульфита натрия. [2]
Возрастание температуры реагирующей смеси влечет за собой резкое увеличение процента активированных молекул, чем, главным образом, и объясняется столь сильное влияние температуры на скорости химических реакций. [3]
Повышение температуры реагирующей смеси за счет экзотермичности реакции составляет Н0 на каждый процент содержания кислорода в газе. [4]
При температуре реагирующей смеси выше 35 вместо крупнокристаллического, легко фильтрующегося осадка углекислого цинка образуется липкая и плохо фильтрующаяся основная соль углекислого цинка. [5]
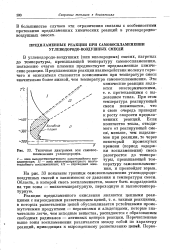 |
Типичная диаграмма зон самовоспламенения углеводородов. [6] |
При этом температура реагирующей смеси повышается, что в свою очередь приводит к росту скорости предпламенных реакций. Если количество тепла, отводимого от реагирующей смеси, меньше, чем выделяемое при реакции, то через некоторый промежуток времени ( период задержки воспламенения) смесь разогреется до температуры, превышающей температуру самовоспламенения, и произойдет взрыв. На рис. 33 показаны границы самовоспламенения углеводородо-воздушных смесей в зависимости от давления и температуры смеси. Область, в которой смесь воспламеняется, может быть подразделена на три зоны - низкотемпературную, переходную ж высокотемпературную. [7]
При повышении температуры реагирующей смеси в системе, наряду с реакцией переписного радикала с углеводородом, приводящей к образованию гидроперекиси, наблюдается, в связи с расслаблением связей в молекуле перекисного радикала, частичный его распад на кислородсодержащее соединение и на новый радикал. Из полученного нами экспериментального материала следует, что переписные радикалы до 200 сравнительно стабильны, в результате чего главным продуктом реакции до этой температуры все еще являются гидроперекиси. [8]
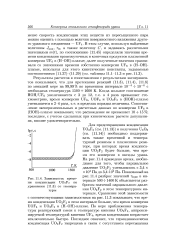 |
Зависимость време - rrvr, ... Anr. T. [9] |
По мере приближения температуры реагирующей смеси к температуре кипения UO2F2, аппроксимируемой температурой кипения UF4, время конденсации возрастает исключительно быстро. [10]
Предполагая, что состав и температура реагирующей смеси постоянны во всем объеме реактора, мы предъявляем очень строгие требования к скорости перемешивания реагирующей смеси. Интересно, однако, попытаться учесть влияние неидеальности смешения на ход процесса. Мы не будем глубоко вдаваться в изучение этого вопроса, который гораздо более тщательно исследован в указанной в конце главы литературе, но только постараемся проиллюстрировать основные идеи. [11]
Для тех случаев, когда температура реагирующей смеси изменяется в достаточно узких пределах, Д. А. Франк-Каменецкий предложил воспользоваться приближенным представлением закона Аррениуса, которое он назвал методом разложения экспоненты. Этот метод заключается в разложении в ряд величины E / ( RT) в окрестности некоторой характерной температуры Ts, вблизи которой идет реакция. Роль Ts, в частности, может сыграть температура, соответствующая стационарному состоянию. [12]
 |
Принципиальная схема установки. [13] |
Это дало следующие преимущества: удобство замера температуры реагирующей смеси; снижение вклада в общий итог гетерогенных реакций, протекающих на стенках; возможность работы в режиме, близком к адиабатическому, что снижает погрешности, связанные с учетом теплопотерь в стенки реактора. [14]
Аналогичным образом, если стационарный разогрев становится невозможным и температура реагирующей смеси начинает возрастать существенно нестационарным образом, то это явление носит название теплового воспламенения. [15]
Страницы: 1 2 3 4