Температура - реагирующая смесь
Cтраница 2
 |
Схематическое изображение ступенчатого адиабатического реактора с промежуточным тсплоотводом.| Изменение температуры определение может явиться пред-по ступеням адиабатического реактора г. [16] |
На рис. 111 - 17 приведен также характер изменения температуры реагирующей смеси в таком реакторе. Наличие проме-жу точного теплообмена между секциями позволяет увеличить температуру реакции на первых ступенях, что обеспечивает высокую скорость реакции при малых степенях превращения и, тем самым, дает возможность существенно уменьшить общий объем реактора, необходимый для достижения заданной конечной степени превращения, по сравнению с одноступенчатым реактором. Особенно важно это для контактно-каталитических процессов, у которых затрат л на катализатор прямо пропорциональны требуемому времени пребывания реагентов в аппарате для его заданной производительности. [17]
Таким образом, существует определенное условие перехода от случая ограниченного повышения температуры реагирующей смеси к случаю, когда ее температура быстро растет и достигает весьма высокого значения, близкого к теоретической температуре горения. [18]
Если при некоторых значениях температуры и давления стационарный разогрев становится невозможным и температура реагирующей смеси начинает возрастать существенно нестационарным образом, то это явление носит название теплового воспламенения. При достаточно низких давлениях выделение тепла в ходе реакции компенсируется теплоотводом; с ростом давления выделение тепла е сосуде увеличивается, что ведет к возрастанию температуры газа и, следовательно, ускорению теплоотдачи. Однако вследствие увеличения температуры возрастают также скорость реакции и скорость выделения тепла. [19]
 |
Прямоугольник без контакта для обобщенной модели реактора непрерывного действия. [20] |
Безразмерные переменные х, у, т пропорциональны соответственно концентрации реагента, температуре реагирующей смеси и времени. Функция f ( x, у) характеризует скорость химической реакции, ( р ( х, у) - скорость тепловыделения. Параметр К пропорционален объемной скорости входного потока; ц определяется условиями теплоотвода; величина х0 пропорциональна концентрации реагента на входе, уо - линейной комбинации температуры смеси на входе и температуры стенки реактора. [21]
Безразмерные переменные х, у, т пропорциональны соответственно концентрации реагента, температуре реагирующей смеси и времени. Функция f ( x y) характеризует скорость химической реакции, ц ( х, у) - скорость тепловыделения. Параметр К пропорционален объемной скорости входного потока, & м ц определяется условиями теплоотво-да; величина х0 пропорциональна входной концентрации реагента, уо - линейной комбинации входной температуры смеси и температуры стенки реактора. Все параметры системы ( К, Ц, - о, У о) положительны. [22]
В предыдущей главе мы видели, как изменяется скорость реакции с изменением состава и температуры реагирующей смеси. [23]
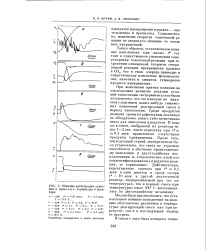 |
Образцы регистрации давления н термо-э. д.с. термопары в реакторе. [24] |
Можно было предположить, что установленное влияние наполнения на реак цию обусловлено различием в температурах реагирующей смеси как при перепуске, так и в последующий период ее прогрева. [25]
Здесь подразумевается, что для обоих стационарных состояний реактора, в которых он поочередно находится, температура реагирующей смеси: неизменна и составляет 28 5 С. [26]
Химическое превращение всегда связано с изменением энтальпии реагентов, выделением или поглощением тепла, что изменяет температуру реагирующей смеси. Возможен теплообмен с окружающей средой. К ней относится и теплоноситель, с помощью которого можно поддерживать желаемые температурные условия в зоне протекания реакции. [27]
Цепные взрывы следует отличать от тепловых взрывов, при которых выделение тепла при экзотермической реакции приводит к увеличению температуры реагирующей смеси и, тем самым, к росту скорости каждой из стадий реакции, что еще больше увеличивает скорость основной реакции и суммарную скорость выделения тепла. [28]
Произведенные им наблюдения показали, что в ходе процесса можно выделить два периода: начальный период, проходящий без изменения температуры реагирующей смеси, и второй период экзотермической реакции, причем подъем температуры происходит вначале медленно, а затем более быстро. Такое течение реакции указывает, что при взаимодействии между фенолом и азотной кислотой имеет место автокаталитический процесс, развитие и протекание которого происходят за счет некоторой промежуточной реакции, являющейся источником образования катализатора. [29]
Произюеденные им наблюдения показали, что в ходе процесса можно выделить два периода: начальный период, проходящий без изменения температуры реагирующей смеси, и второй период экзотермической реакции, причем подъем температуры происходит вначале медленно, а затем более быстро. Такое течение реакции указывает, что при взаимодействия между фенолом и азотной кислотой имеет место автокаталитический процесс, развитие и протекание которого происходят за счет некоторой промежуточной реакции, являющейся источником образования катализатора. [30]
Страницы: 1 2 3 4