Критическая температура - вода
Cтраница 1
Критическая температура воды равна 374; этой температуре соответствует давление р - 225 ата. [1]
Критическая температура воды равна 374 0 С, критическое давление - 221 4 атм ( эталонное давление) и критический объем - 45 мл / моль. [2]
 |
Схема обогрева перегретой водой с естественной циркуляцией. [3] |
Нагревание перегретой водой Критическая температура воды равна 374; этой температуре соответствует давление р225 ата. [4]
Определим критическую толщину льда и критическую температуру воды, при которых произойдет полное замерзание воды в трубе при данных условиях. [5]
При температурах, близких к критической температуре воды, невозможно обнаружить проявление каких-либо элементов квазикристалличности. Однако в обычных условиях, в которых определяется теплота гидратации, квазикристаллическая структура должна иметь существенное значение для энергетики процесса гидратации. Эта идея была впервые высказана Берналом и Фаулером, а затем ими и многими другими авторами использовалась при расчете теплот гидратации. [6]
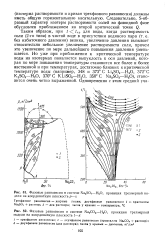
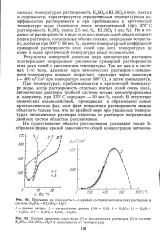
Но уже при приближении к критической температуре воды на изотермах появляется выпуклость к оси давлений, которая по мере повышения температуры становится все более и более явственной и при температурах, достаточно близких к критической температуре воды ( например, 348 и 373 С Li2SO4 - H2O, 372 С K2SO4 - H2O, 370 С KLiSO4 - Н2О, 350 С Na4SO4 - Н2О), становится очень четко выраженной. [8]
При температурах, приближающихся к критической температуре воды, когда растворимость отдельно взятых солей очень мала, эвтонические растворы тройной системы весьма концентрированны и, например, при 370 С содержат - 50 вес. В отсутствие химических взаимодействий, приводящих к образованию новых кристаллических фаз, этот факт повышения растворимости можно объяснить только тем, что по крайней мере при указанных температурах эвтонические растворы отделены от растворов пограничных двойных систем областью расслаивания. [10]
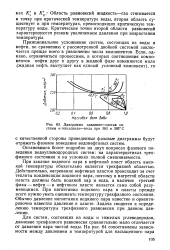 |
Диаграмма давление-состав системы w - гексадекан-вода при 363 и 365 С. [11] |
Область равновесий жидкость-газ стягивается в точку при критической температуре воды, вторая область существует и при температурах, превосходящих критическую температуру воды. Критические точки второй области равновесий характеризуются резким увеличением давления при возрастании температуры. [12]
Последняя при температурах, почти совпадающих с критической температурой воды, переходит в надкритическое состояние. [13]
Однако диапазон рабочих температур здесь резко ограничен значениями критических температур воды - 374 С и этанола - 243 С. Только в этом узком интервале температур ( 243 - 374 С) термодинамически могут сосуществовать газообразный этанол и жидкая вода. Чтобы вода не испарялась, давление должно быть, очевидно, выше критического давления воды, которое при / 374 С составляет 21 7 МПа. Критическая температура этилена 9 7 С значительно меньше и не определяет рабочей температуры процесса. [14]
У каждого вещества имеется своя критическая температура ( например, критическая температура воды 374 С, кислорода - 118 С, водорода - 240 С, гелия - 268 С. [15]
Страницы: 1 2 3 4