Критическая температура - вода
Cтраница 3
 |
Диаграмма давление-состав системы w - гексадекан-вода при 363 и 365 С. [31] |
Область равновесий жидкость-газ стягивается в точку при критической температуре воды, вторая область существует и при температурах, превосходящих критическую температуру воды. Критические точки второй области равновесий характеризуются резким увеличением давления при возрастании температуры. [32]
 |
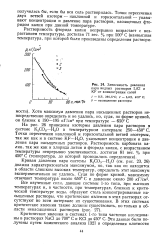
Политерма растворимости Li 2СО3 в воде. [33] |
На рис. 5 видно, что растворимость Li2CO3 в воде с повышением температуры непрерывно уменьшается, при приближении к критической температуре воды выражается лишь сотыми долями процента. [34]
 |
Зависимость давления пара водных растворов LiCl и KF от концентрации солей. [35] |
Все изученные соли, дающие системы 1-го типа, при высоких температурах и, в частности, при температурах, близких к критической температуре воды, образуют столь концентрированные насыщенные растворы, что критические явления в этих растворах отсутствуют во всем интервале их существования. [36]
 |
Параметры, соответствующие второй критической точке Q. [37] |
Относительно невысокие pq ( около ЮООкГ / сж2) и значительные CQ ( 30 - 40 %) доказывают возможность получения при температурах, превышающих критическую температуру воды, и при не столь уж высоких давлениях высококонцентрированных флюидных и жидких растворов солей, растворимость которых при тех же температурах, но при более низких давлениях очень незначительна. [38]
Характерной особенностью этого вида солей является то, что при достаточно высоких температурах им свойствен уже отрицательный температурный коэффициент растворимости, и при приближении к критической температуре воды растворимость этих солей становится совсем незначительной. [39]
Это можно осуществить разными путями, а частности следующими четырьмя приемами: 1) нагреть водяной пар, оставляя давление неизменным, до температуры, превышающей критическую температуру воды; 2) затем сжать перегретый водяной пар давлением, превышающим критическое давление; 3) вновь охладить перегретый и сжатый водяной пар до температуры Т, сохраняя давление неизменным; 4) наконец, снизить давление до заданного значения 1 ат. [40]
Приводимые в литературе диаграммы растворимости таких хорошо известных солей, как сульфаты натрия, калия, карбоната натрия, обычно заканчиваются при температуре, близкой к критической температуре воды, так как растворимость этих солей вблизи 374 С при давлениях, равных давлению пара растворов, чрезвычайно мала. Но результаты изучения фазовых равновесий в системах Na2SO4 - H2O, K2SO4 - H2O, Li2SO4 - H2O, Na2CO3 - Н2О, KLiSO4 - H2O доказывают существование при высоких температурах и давлениях весьма концентрированных растворов исследованных солей. В соответствии с этим диаграммы растворимости сульфатов натрия, калия, лития и карбоната натрия должны быть дополнены фазовыми равновесиями в околокритической и надкритической областях. Именно в этих областях исключительный интерес представляет вопрос о влиянии на растворимость солей такого важного фактора равновесия, как давление. [41]
Авенариусом и рядом его учеников, особенно Надеждиным Зайончевским и др., были определены критические параметры многих жидкостей, в том числе Надеждиным и Страусом была определена различными методами критическая температура воды. [42]
Ингерсон [3] указывал, что такого поведения нужно было ожидать для включения, состоящего при комнатной температуре из воды и пара в определенном отношении ( около 3: 7) и затем нагретого до критической температуры воды. В рассматриваемых включениях система является не такой простой, но принцип, повидимому, сохраняется. [43]
Но уже при приближении к критической температуре воды на изотермах появляется выпуклость к оси давлений, которая по мере повышения температуры становится все более и более явственной и при температурах, достаточно близких к критической температуре воды ( например, 348 и 373 С Li2SO4 - H2O, 372 С K2SO4 - H2O, 370 С KLiSO4 - Н2О, 350 С Na4SO4 - Н2О), становится очень четко выраженной. [44]
По данным Тренева и Григорович [24], жидкие водные растворы сульфатов натрия и калия и трехзамещенного фосфата натрия существуют при давлении водяного пара 300 am и при температурах ( 380 и 400), превышающих критическую температуру воды. [45]
Страницы: 1 2 3 4