Тетрагалогениды
Cтраница 2
Тетрагалогениды углерода имеют то сходство с чистыми галогенами, что комплексообразующими атомами в них являются атомы галогена. Как и в некоторых комплексах, обсуждавшихся выше, сдвиг частоты ЯКР брома невелик и имеет величину порядка сдвига под влиянием окружающей среды, который обусловлен межмолекулярным взаимодействием и наличием движений; однако заслуживает упоминания следующий факт, на который обращается внимание в работе [70]: хотя влияние переноса заряда на резонанс брома настолько мало, что его нельзя отличить от межмолекулярных вкладов, перенос заряда все же наблюдается методом УФ-спектроскопии в родственных комплексах тетрахлорида углерода. Напомним также высказанное о малости сдвига резонанса брома в комплексе 2CH3GN Вг2 замечание о том, что акцептирующие rf - орбитали атома брома характеризуются меньшей ККВ, чем р-орбитали, обычно рассматриваемые при обсуждении образования связи. Среди комплексов галогенмета-нов методом ЯКР наиболее широко исследовались комплексы хлороформа. [16]
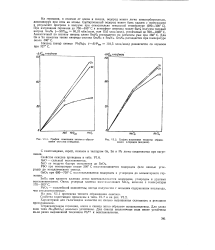 |
График изменения теплоты образования окислов ( твердых.| График изменения теплоты образования хлоридов ( жидких. [17] |
Тетрагалогениды германия, олора и свинца легко образуют ацидокомплексы. Для олова соли типа Me2 [ SnCleJ довольно устойчивы. Для свинца аналогичные соли менее устойчивы из-за резко выраженной тенденции РЬ4 к восстановлению. [18]
Тетрагалогениды титана алкилируются рядом реакционно-способных металлоорганических соединений. Наиболее хорошо охарактеризованными продуктами являются метилтитантри-хлорид и метилтитантрибромид, а также диметилтитандихлорид. [19]
Тетрагалогениды ванадия легко гидролизуются. [20]
Тетрагалогениды олова в донорных растворителях могут координировать две донорные молекулы. Из данных ЯКР-81Вг в тетрабромиде олова было установлено, что в диэтиловом эфире, диоксане, пиридине и диметилсульфоксиде образуются транскомплексы, тогда как uc - комплексы образуются в гексаметилфосфор-триамиде. Дальнейшее применение метода ЯКР-спектроскопии в этой области обещает дать новые результаты. [21]
Тетрагалогениды титана характеризуются пониженными значениями температур плавления и кипения, отчетливо выраженной склонностью к гидролизу ( за исключением тетрафторида), к ком-плексообразованию с гидроокисями или галогенидами щелочных металлов. [22]
Смешанные тетрагалогениды типа CF2C12, CF3C1 и другие используют в качестве фреонов. Твердые при обычных условиях СВг4 и С14 применяют редко. Большое значение имеют хлор-и фторпроизводные разнообразных полимерных углеводородов. Эти пластмассы разнообразны и ценны по свойствам. Их широко используют в бытовых и производственных целях. [23]
Тетрагалогениды молекулярной структуры летучи, химически активны. [24]
Тетрагалогениды металлов подгруппы титана, за исключением TiF4, ZrF4, растворяясь в воде, гидролизуются, образуют аддукты с аммиаком, пиридином, анилином или другими аминами, а также с РС13, РОС13, РС15 и др. Они образуют также комплексные соли с галогенидами щелочных металлов. [25]
Безводные тетрагалогениды других элементов подгруппы титана и на влажном воздухе, и попадая в воду также сильно гидролизуются. С ними необходимо работать в тщательно высушенной атмосфере сухой камеры или в шленк-аппаратуре. В наименьшей степени гидролизуются тетрагалогениды тория. Гидратированные ( но не гидролизо-ванные) соединения состава ТпГ4 - пН2О можно получить кристаллизацией из Н2О, если в систему добавить НГ для подавления гидролиза. [26]
Известны тетрагалогениды MnF4 и МпС14, характеризующиеся малой устойчивостью. В отличие от этих тетрагалогенидов ацидо-соли типов МеЧМпХ5 ], МеНМпХ01 ( где X F -, С1 -, CN -) значительно более устойчивы. [27]
Все тетрагалогениды образуют комплексные анионы типа [ TiHlge ] 2 -, где Hlg - галоген. Наиболее устойчивыми соединениями являются соли гексафторотитановой кислоты H2 [ TiF6 ]; калиевая и натриевая соли этой кислоты применяются при крашении кожи. [28]
Все тетрагалогениды ЭГ4 гигроскопичны, а большинство из них ( кроме полимерных фторидов) легко гидролизуются. Так как основный характер гидроксидов Э ( ОН) 4 при переходе от титана к цирконию и гафнию несколько усиливается, степень гидролиза галоге-нидов в этом же ряду уменьшается. [29]
Все тетрагалогениды ЭГ4 под действием галоводородов или галогенидов образуют комплексные галогенкислоты Н2 [ ЭГ6 ] или галогенсоли Ме. [30]
Страницы: 1 2 3 4