Тетрагалогениды
Cтраница 4
Фосфор и мышьяк образуют так называемые тетрагалогениды Р2С14, РЛ4 и As. LP-PL с транс-новоротпой ориентацией в твердом состоянии [ 5i, но, возможно, в растворе CS. Mil одна из PL-групп выполняет колебательно-вращательные движения относительно другой группы ( подобно N. [46]
Фосфор и мышьяк образуют так называемые тетрагалогениды Р2С14, РЛ4 и As. Оказывается, что РЛ4 имеет молекулярную структуру 12Р - Р12 с транс-поворотной ориентацией в твердом состоянии 15 ], но, возможно, в растворе CS. PI-групп выполняет колебательно-вращательные движения относительно другой группы ( подобно N2H4 стр. [47]
Существуют и термодинамически устойчивы все бинарные тетрагалогениды кремния: фторид кремния SiF4 - бесцветный газ, хлорид кремния SiCl4 и бромид кремния SiBr4 - бесцветные жидкости, иодид кремния SiI4 - бесцветное кристаллическое вещество. Электронные орбитали атомов кремния в тетраэдрических по структуре молекулах тетрагало-генидов проявляют зр3 - гибридизацию. [48]
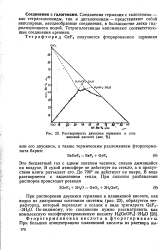 |
Растворимость двуокиси германия в плавиковой кислоте ( вес. %. [49] |
Соединения германия с галогенами - как тетрагалогениды, так и дигалогениды - представляют собой неполярные, несолеобразные соединения, в большинстве легко гид-ролизующиеся водой. Тетрагалогениды напоминают соответствующие соединения кремния. [50]
Легко реагирует с галогенами, образуя тетрагалогениды. [51]
К галогенидам циркония и гафния относятся тетрагалогениды, продукты присоединения к ним, продукты замещения, галогеноцирконаты и гафнаты и галогениды низших валентностей. Наиболее прочные из них соединения с фтором, наименее прочные - соединения с иодом. [52]
Страницы: 1 2 3 4