Тетраоксид
Cтраница 1
Тетраоксид, триоксид сурьмы и сурьмяно-силикатное стекло применяются при диффузии в кремний методом открытой трубы с использованием азота как транспортирующего газа. [1]
Тетраоксид ОзО4 обладает резким неприятным запахом; ДС59В - 302 2 кДж / моль; Х в 137 Дж / ( моль - К) ( см. также табл.); давление пара 66 5 Па ( 0 О, 532 Па ( 23 С), 27 3 кПа ( 91 С); р-римость ( г в 100 г): в воде 5 7 ( 10 С), 6 23 ( 25 С), в СС14 - 250 ( 20 С); раств. ОН) 2 ]; сильный окислитель; получают при нагр. С зО4 используют для окраски биол. [2]
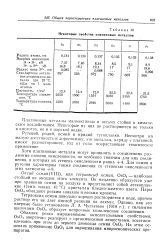 |
Некоторые свойства платиновых металлов. [3] |
Тетраоксид осмия довольно хорошо растворяется в воде, причем раствор его не дает кислой реакции на лакмус. Однако, как это впервые было установлено Л. А. Чугаевым ( 1918 г.), с сильными щелочами OsO4 образует непрочные комплексные соединения. [4]
Тетраоксид осмия довольно хорошо растворяется в воде, причем раствор его не дает кислой реакции на лакмус. Однако, как это впервые было установлено Л. А. Чугаевьш ( 1918 г.), с сильными щелочами Os04 образует непрочные комплексные соединения. [5]
Тетраоксид осмия катализирует реакцию иодата с мышьяком или сульфатом гидразина в щелочных средах. [6]
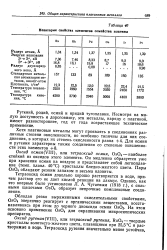 |
Некоторые свойства элементов семейства платины. [7] |
Тетраоксид осмия довольно хорошо растворяется в воде, причем раствор его не дает кислой реакции на лакмус. Однако, как это впервые было установлено Л. А. Чугаевым ( 1918 г.), с сильными щелочами OsO4 образует непрочные комплексные соединения. [8]
Тетраоксиды осмия и рутения очень ядовиты. Его используют как мягкий окислитель и катализатор в органическом синтезе ( например, кортизона) и для подкрашивания животных тканей при их микроскопическом исследовании. [9]
Тетраоксид осмия довольно легко образуется при окислении осмия или его соединений кислородом, азотной кислотой и другими окислителями. [10]
Тетраоксиды ссмия и рутения ядовиты. Его используют как мягкий окислитель и катализатор в органическом синтезе ( например, кортизона) и для подкрашивания животных тканей при их микроскопическом исследовании. [11]
Тетраоксид осмия [5.1258], хромат [5.1200] и диоксид марганца [5.1238] ускоряют окисление хлоратами, однако, они широко не используются. [12]
Тетраоксид осмия довольно легко образуется при окислении осмия или его соединений кислородом, азотной кислотой и другими окислителями. [13]
Тетраоксиды осмия и рутения ядовиты. Его используют как мягкий окислитель и катализатор в органическом синтезе ( например, кортизона) и для подкрашивания животных тканей при их микроскопическом исследовании. [14]
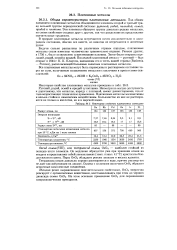 |
Некоторые свойства платиновых металлов. [15] |
Страницы: 1 2 3 4