Тетраоксид
Cтраница 3
Тетраоксид осмия довольно хорошо растворяется в воде, причем раствор его не дает кислой реакции на лакмус. Однако, как это впервые было установлено Л. А. Чугаевым ( 1918 г.), с сильными щелочами OsO4 образует непрочные комплексные соединения. [31]
Выделен газообразный тетраоксид ксенона ХеО4 - самое летучее соединение ксенона. [32]
Молекула тетраоксида имеет форму тетраэдра с атомом Хе в центре. В твердом состоянии взрывается даже при - 40 С. [33]
Молекула димера - тетраоксида диазота N2O4 - плоская. При 22 С N2O4 конденсируется в жидкость, при - 11 С - замерзает. [34]
Рутений и осмий образуют тетраоксиды RuO4 и OsO4, которые представляют собой типичные молекулярные соединения ( температуры плавления 25 и 40 С соответственно) с заметными окислительными свойствами. В то же время оксиды МО, характерные почти для всех элементов первого переходного ряда, отсутствуют в третьем ряду. [35]
Крите в 1936 г. Тетраоксид осмия представляет собой бесцветное кристаллическое вещество, хорошо растворимое в эфире, диоксане, пиридине и других органических растворителях. При взаимодействии тетраоксида осмия с алкенами в эфире или диоксане образуется черный осадок циклического эфира осмиевой кислоты - осмат, который легко может быть изолирован в индивидуальном виде. Присоединение OsC4 к двойной связи заметно ускоряется в растворе пиридина. [36]
Очень активным реагентом является тетраоксид рутени. Бензол, относительно устойчивый к действию дихромата или перманганата, с Rup4 реагирует со взрывом. Разработаны методики окисления каталитическими количествами этого реагента в сочетании с Nal64 или NaCIO в двухфазной системе. [37]
Ввиду токсичности и летучести тетраоксида осмяя во время этой операции необходимо соблюдать соответствующие мери предосторожности. [38]
Для рутения и осмия известны тетраоксиды. [39]
Соединения с п 4 - тетраоксиды ROOOOR - являются интермедиатами инициированного окисления или автоокисления органических соединений молекулярным кислородом. Тетраоксиды образуются на стадии обрыва цепи окисления в результате рекомбинации пероксильных радикалов. Наиболее устойчивыми являются третичные тетраоксиды, которые стабильны при температурах ниже - 100 С. [40]
Катализатором реакции может быть также тетраоксид осмия. [41]
Например, рутений, имея в тетраоксиде RuO4 восемь ковалент-ных связей с атомами кислорода за счет 4d5 -, 5s - и 5р2 - электронов, вступает еще в связь с триэтилфосфором Р ( С2Н5) 3, акцептируя от него пару электронов своей третьей 5р - орбиталью. [42]
Например, рутений, имея в тетраоксиде RuCu восемь ковалентных связей с атомами кислорода за счет 4d5 5s и 5р - электронов, вступает еще в связь с триэтил-фосфором Р ( С2Н5) з, акцептируя от него пару электронов своей третьей 5р - орби-талью. [43]
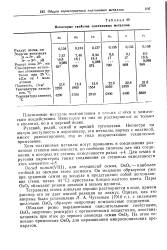 |
Некоторые свойства платиновых металлов. [44] |
Оксид ослшя ( УШ), или тетраоксид осмия, OsO4 - наиболее стойкий из оксидов этого элемента. Он медленно образуется уже при хранении осмия на воздухе и представляет собой легкоплавкие ( темп, плавл. [45]
Страницы: 1 2 3 4