Тетраоксид
Cтраница 2
Тетраоксид осмия довольно хорошо растворяется в воде, причем раствор его не дает кислой реакции на лакмус. Однако с сильными щелочами Os04 образует непрочные комплексные соединения. [16]
 |
Структуры молекул NU2 ( а и N20 ( б ( межатомные расстояния приве. [17] |
Тетраоксид диазота N204 образует бесцветные кристаллы ниже - 11 С. [18]
Тетраоксид осмия имеет слабые кислотные свойства. [19]
Тетраоксид осмия ( OsO4) - летучий твердый продукт, кристаллизующийся в белые игольчатые кристаллы; он действует на глаза и легкие; используется в гистологии и микрографии. Тетраоксид дает осматы такие, как осмат калия ( красные кристаллы), а при обработке аммиаком и гидрооксидами щелочных металлов, осмиаматы такие, как осмиамат калия или натрия, представляющие собой желтые кристаллы. [20]
Тетраоксид осмия растворим в воде, причем его молекула не претерпевает существенных изменений. [21]
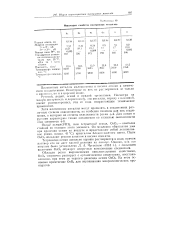 |
Некоторые свойства платиновых металлов. [22] |
Тетраоксид осмия довольно хорошо растворяется в воде, причем раствор его не дает кислой реакции на лакмус. Однако, как это впервые было установлено Л. Л. Чугаевым ( 1918 г.), с сильными щелочами OsO4 образует непрочные комплексные соединения. [23]
Тетраоксид осмия образуется при окислении порошкообразного осмия или его соединений кислородом, азотной кислотой и другими окислителями. Оксид осмия ( VIII) растворим в воде, но определенных соединений при этом не образует. Кислотные свойства OsO4 проявляет при взаимодействии с основными соединениями. [24]
Тетраоксиды осмия и рутения ядовиты. Его используют как мягкий окислитель и катализатор в органическом синтезе ( например, кортизона) и для подкрашивания животных тканей при их микроскопическом исследовании. [25]
Тетраоксид осмия - дорогой и труднодоступный реагент, к тому же он очень токсичен. Поэтому оксид осмия ( VIII) используют для синтеза малых количеств труднодоступных веществ с целью получения наиболее высокого выхода диола. Для упрощения сш-гидроксилирования алкенов под действием OsCu была разработана методика, позволяющая использовать лишь каталитические количества этого реагента. [26]
Тетраоксид осмия довольно легко образуется при окислении осмия или его соединений кислородом, азотной кислотой и другими окислителями. [27]
Тетраоксид висмута может быть получен окислением металлического висмута, ВЮ или Bi2Oj озоном или пер-манганатом калия, а также в результате сплавления В12Оз с избытком щелочи. [28]
Тетраоксид осмия дает очень хорошие выходы. В присутствии лероксида водорода можно обойтись каталитическим количеством тетраоксида осмия, так как образующийся триоксид окисляется до тетраоксида. [29]
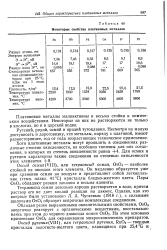 |
Некоторые свойства платиновых металлов. [30] |
Страницы: 1 2 3 4