Трифениламин
Cтраница 2
Трифениламин ( C H5) N - кристаллическое вещество, не растворимое в воде и имеющее совершенно нейтральный характер. [16]
Даже трифениламин и трифенилфосфин, которые обычно считаются очень слабыми основаниями, в серной кислоте ведут себя как сильные основания. [17]
Молекула трифениламина плоская, иначе невозможно было бы р, я-сопряжение. При нарушении плоскостной структуры основность азота возрастает. Виттигу удалось, отнимая НС1 от 9 - ( о-хлорфенил) - 9 10-дигидроакридина посредством NaNH2 в жидком аммиаке, замкнуть пространственный гетероцикл - азатриптицен. [18]
Гидрофторид трифениламина ( CeH5) 3NHF образуется из амина и концентрированного спиртового раствора HF. Гидрофторид дифениламина ( C6H5) 2NH - 2HF образуется в водном растворе, однако ( C6H5) 2NH - 3HF можно получить лишь из спиртового раствора HF; гидрофторид азобензола ( CeH5) 2N2 - HF получается также в спиртовом растворе. Примерами могут служить: анилин, о -, м - и п-толуидин, м - и л-нитроанилин, ж-ксилидин, цимидин, ф-кумидин, о-толидин, дифениламин, трифенилгуанидин, п-фенетидин, о-анизидин, п-нитро-о-ани - зидин, а - и p - C10H NH2, иод-о-толуидин, антраниловая кислота, фенилме-тиламин, фенилэтиламин, метаниловая кислота и сульфаниловая кислота. При титровании растворов этих соединений едким натром с индикаторами при рН больше 6 удается оттитровать только три четверти связанной кислоты. [19]
Производные трифениламина, содержащие в бензольных ядрах диметиламино - или оксигруппы, обладают большой лабильностью и не могут быть приготовлены обычными способами. [20]
Например, трифениламин дает с комплексом 58 % дифениламина, а с литием только 8 % дифениламина. [21]
За исключением трифениламина, о металлировании которогс было сказано выше и который металлируется в и ега-положение, простые третичные ароматические амины металлируются в орто-положение. [22]
Для получения более чистого трифениламина сырой продукт растворяют при кипячении с обратным холодильником приблизительно в 700 мл уксусноэтилового эфира. Полученный раствор быстро охлаждают при перемешивании, причем амин выделяется в виде почти бесцветных кристаллов. [23]
Замечательно, что трифениламин не имеет дипольного момента, следовательно, представляет собой плоскую молекулу. [24]
Третичные амины ( трифениламин н др.) образуют с Т.е. комплексы с переносом заряда. [25]
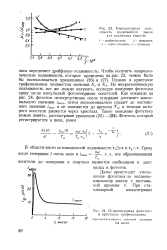 |
Температурная зависимость подвижности дырок.| Осциллограмма фототек.. i i в кристалле трифениламина. [26] |
Однако в кристалле трифениламина неизвестны значения Nc и Nn. [27]
Природа и стабильность катион-радикалов три-лара-заме-щенных трифениламинов ( так называемых аминиевых ионов или аминиевых радикалов), например ТАА, три-л-бромфенил-амина ( ТБФА) и три-л-толиламина ( ТТА), также определены методом ЭПР. Интенсивность ЭПР-спектров этих соединений практически не изменяется со временем. Стабильность пара-за-мещенных триариламиниевых ионов частично обусловлена резонансной стабилизацией и лишь частично - ингибированием сочетания бензидинового типа вследствие блокирования пара-положений арильных групп путем введения заместителей. Действительно, анодное окисление ряда триариламинов, не замещенных по пара-положению арильной группы, сопровождается образованием бензидина. [28]
Трис-азокрасители 95 Тритил см. Трифенилметил Трифениламин 76, 82, 83 Триоениламиногуанидин 290 Триоенилацилфосфоний 488 Триоенилбензол 17, 135 Трифенилгалоидметаны 205 Трифенилдибензоилметилфосфоний 391 Трифенилен 59, 187, 242, 243 Три-о-фенилендиарсин 403 Трифенилметан 192, 193 ел. [29]
Чисто ароматические амины, например трифениламин, взаимодействуют с азотистой кислотой в присутствии концентрированной серной кислоты с образованием красителей синего цвета. Строение этих продуктов еще недостаточно выяснено. [30]
Страницы: 1 2 3 4