Трифенилбромметан
Cтраница 2
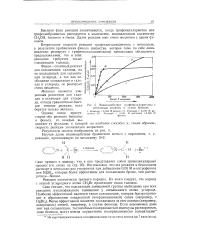 |
Взаимодействие, трифенилхлорметана с метиловым спиртом в сухом бензоле. [16] |
Быстрая фаза реакции заканчивается, когда трифенилхлорметан или трифенилбромметан расходуется в количестве, эквивалентном количеству СН3ОН, бывшего в смеси. Далее реакция идет очень медленно с одним фенолом. [17]
Какими свойствами обладает вещество, получаемое действием серебра на трифенилбромметан. [18]
Дифенилбромметан, 2-бром - 2-фенилпропан, 2-бром - 2-ме-тилпропан и трифенилбромметан нагревают в водной муравьиной кислоте. [19]
Вещество не реагирует с полухлористой медью, йодистым метилом, четыреххлористым углеродом, трифенилбромметаном. [20]
В этом случае можно получить органический катион при действии хлорного олова, подобно тому как получают катион трифенилбромметана. [21]
Первый свободный радикал с трехвалентным углеродом был открыт в 1900 Гомбергом при попытке синтеза гексафенилэтана действием молекулярного серебра на трифенилбромметан. [22]
Однако при действии трифепилбромметапа в тех же условиях на диэтилфосфористый натрий вся картина реакции протекала совершенно иначе: при прилипании по каплям бензольного раствора трифенилбромметана к эфирному раствору диэтилфосфористого натрия содержимое колбы быстро окрашивалось в желто-оранжевый цвет. [23]
Нафтиленалкиловые эфиры фосфористой кислоты, за исключением фенилового и аллилового эфиров, легко перегруппировываются по схеме А. Е. Арбузова при нагревании до 170 - 180 эквимолекулярных количеств эфиров с трифенилбромметаном с выделением соответствующего алкил-бромида и образованием хорошо кристаллизующегося эфира трифепилме-тилфосфинрвой кислоты. [24]
Выпадение бромистого натрия началось, когда была слита треть раствора. После того как весь раствор трифенилбромметана был слит, колба в течение 5 мин. Затем через воронку было прибавлено несколько капель воды для свертывания тонкого хлопьевидного осадка бромистого натрия. [25]
О-ацетил-б - О-трифенилметил-р - в-глюкопи-ранозы ( III) растворяют при нагревании на водяной бане в 200 мл ледяной уксусной кислоты. Прибавляют 18 s насыщенного раствора сухого бромистого водорода в ледяной уксусной кислоте, смесь встряхивают - 45 сек, выпавший трифенилбромметан немедленно отфильтровывают с отсасыванием. Маточный раствор выливают в - 1 л смеси воды со льдом или непосредственно фильтруют в эту смесь. Тетраацетат экстрагируют 250 мл хлороформа, экстракт четырежды промывают водой с температурой 0 для удаления уксусной кислоты и высушивают безводным сульфатом натрия. Осушитель отфильтровывают и раствор упаривают в вакууме при комнатной температуре. Остаток заливают 100 мл безводного эфира, растирая сироп стеклянной палочкой. [26]
Если подвижность хлора в ( С6Н5) зСОС1 обусловлена отрицательным характером трех групп C6Hs, то и трибензоилбромметан ( С6Н5СО) 3СВг должен быть также неустойчивым, так как бензоильная группа должна быть по крайней мере так же отрицательна, как и фенильная. Однако опыт показывает, что это совсем не так; можно нагревать трибензоилбромметан в течение нескольких часов со спиртом без того, чтобы в нем произошли какие-либо изменения, тогда как трифенилбромметан в гех же условиях теряет количественно свой бром. [27]
Бензиловый эфир этиленгликольфосфористой кислоты, так же как и бепзиловые эфиры триметиленгликольфосфористой и а-метилтриметилен-гликольфосфористой кислот, при взаимодействии с галоидными соединениями не размыкает цикла. При реакции с хлористым и бромистым бензилом получены эфиры бепзилфосфиновой кислоты и соответствующих гли-колей. Взаимодействием бензиловых эфиров с трифенилбромметаном получены циклические эфиры трифенилметилфосфиновой кислоты. [28]
Образование свободных триарилметильных радикалов стимулируется действием света. Это доказано [101] на примере диссоциации триарилметилбромидов. При освещении солнечным или ультрафиолетовым светом раствор трифенилбромметана окрашивается в ярко-желтый цвет - признак появления свободного трифенилметила. [29]
Из бензола он кристаллизуется с молекулой кристаллизационного бензола, которую при нагревании теряет. Благодаря влиянию фенильных групп атом водорода при третичном атоме углерода обладает особенно высокой реакционной способностью. Он легко окисляется, превращаясь в соответствующий спирт-трифенилкарбинол ( СвНБ) зСОН; при хлорировании и бромировании он превращается в трифенилхлор-метан и трифенилбромметан. [30]
Страницы: 1 2 3