Кристаллический адсорбент
Cтраница 2
На рис. 2 изображена схема прибора, примененного нами для изучения адсорбции паров на кристаллических адсорбентах. Вообще говоря, во многих случаях в приборе достаточно иметь один дозер. [16]
Приведенные в этом разделе результаты сопоставления теоретических расчетов с экспериментальными данными показывают, что в настоящее время термодинамические характеристики удерживания углеводородов кристаллическими адсорбентами могут быть рассчитаны количественно. [17]
Наконец, говоря о характере поверхности твердого ( кристаллического) адсорбента, необходимо иметь в виду, что тот однородный вид поверхности кристаллического адсорбента, который при изложении теории мономолекулярного слоя дан нами на рис. 12 ( стр. На самом деле поверхность эта весьма неоднородна и имеет множество заостренных выступов ( пиков), на которых частицы должны иметь еще более нескомпенсированные силовые поля и линии, чем в идеальной плоскости. С другой стороны, на такой поверхности несомненно должны быть и мельчайшие впадины, углубления, щели, в которых, наоборот, частицы должны находиться в более компенсированном состоянии. Словом, характер твердой поверхности, как стерический фактор, не учитываемый теорией, должен играть серьезную роль в адсорбционных процессах. [18]
В рамках решеточной теории принимается также, что активными центрами могут быть не только некоторые точки адсорбирующей поверхности ( например, узлы решетки кристаллического адсорбента), но и уже адсорбированные молекулы поглощаемого компонента. Это позволяет использовать решеточные теории и для описания так называемой полимолекулярной адсорбции, при которой на поверхности адсорбента образуется не мономолекулярный, а полимолекулярный слой адсорбата. [19]
Простейшим адсорбентом для разделения гомологов, структурных изомеров и вообще молекул, различающихся по их геометрии, а также для разработки количественной молекулярно-ста-тистической теории адсорбционной хроматографии является одноатомный кристаллический адсорбент с однородной плоской поверхностью. [20]
Кристаллические адсорбенты, на поверхность которых выходят несколько ( часто однако немного, не более двух, трех) физически однородных граней разных индексов, можно рассматривать как смесь разных адсорбентов с физически однородными поверхностями. Если различные грани значительно различаются по заселенности атомами, ионами или молекулами, то межмолекулярные взаимодействия таких граней с адсорбирующимися молекулами сильно различаются по потенциальной энергии. Адсорбция на отдельных гранях таких кристаллов при достаточно низких температурах может происходить в основном по очереди на каждой из граней, соответственно, при разных величинах давления пара адсорбата в газовой фазе. [21]
Теория адсорбции Лэнгмюра [25] пренебрегает силами кохезии, действующими в присутствии адсорбирующих сил, но обращает внимание на ненасыщенные остаточные валентности и свободные силы поверхностных атомов, которые должны были бы в противнем случае участвовать в построении кристаллической решетки. В случае кристаллического адсорбента остаточные валентности равномерно распределены по поверхности и расположение их зависит от пространственной решетки. В местах положения свободных валентных сил находится сравнительно небольшое число атомов или атомных групп адсорбента. Адсорбированное вещество удерживается вторичными ( побочными) валентностями ионов, так что адсорбент образует до некоторой степени настоящее химическое соединение с адсорбируемым веществом. [22]
Ими изучено изменение в алюмосиликатом геле на разных стадиях кристаллизации цеолитов при помощи электронного микроскопа, влияние ультразвука на процесс кристаллизации цеолита, влияние дисперсности связующего на прочность и активность гранул цеолита. В результате этих исследований получены новые гелеобразные и кристаллические адсорбенты и установлены важные закономерности адсорбции на этих поглотителях. [23]
Сюда относится, во-первых, создание близких к однородным непористых и пористых кристаллических адсорбентов, во-вторых, накопление надежных и воспроизводимых значений термодинамических характеристик адсорбции на таких адсорбентах и, в-третьих, использование электронных вычислительных машин. Это позволило выразить многие термодинамические свойства системы адсорбат - адсорбент в виде физико-химических констант, характеризующих межмолекулярные взаимодействия адсорбат - адсорбент и адсорбат - адсорбат в адсорбционных системах. Эти воспроизводимые физико-химические константы служат объектами молекулярно-статисти-ческого расчета. [24]
Количественные молекулярно-статистические расчеты коэффициентов / Ci и / С2 в случае газо-адсорбционной хроматографии на достаточно однородных поверхностях кристаллических адсорбентов проще, чем для газо-жидкостной хроматографии, так как силовые центры адсорбента закреплены в кристаллической решетке. [25]
С этой точки зрения благоприятное воздействие адсорбции паров воды можно было попытаться объяснить созданием электронных уровней захвата, задерживающих быструю рекомбинацию электрона с положительным центром, из которого он был удален. Однако этому противоречит тот факт, что в упомянутых выше случаях требовалась вода в капиллярно-жидком состоянии с сопутствующим переходом ионов кристаллического адсорбента в раствор. [26]
Эти выражения для / d не связаны с какими-либо моделями локализованной или подвижной адсорбции. Однако они получены при допущении, что взаимодействие с молекулой адсорбата не изменяет состояние адсорбента, который рассматривается лишь как источник поля межмолекулярных сил, вызывающих вблизи поверхности отклонение состояния газа от идеального состояния. Для кристаллических адсорбентов, в особенности при неспецифической адсорбции, это допущение справедливо. [27]
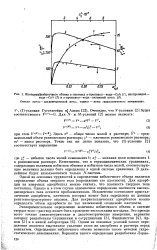 |
Изотермы избыточного объема в системах и-пропанол-вода - СаА ( 1, изопропанол. [28] |
Для адсорбции на инертных адсорбентах можно считать, что плотность твердого тела постоянна. Однако и в этом случае однозначное определение плотности высокодисперсного тела остается проблематичным. Исключение составляют кристаллические адсорбенты, плотность которых может быть определена по данным рентгеноструктурного анализа. [29]
С точки зрения рентгенографических методов исследования пористые адсорбенты могут быть разделены на два класса. К первому относятся системы, в которых практически отсутствует поверхность раздела, и где стенки полостей или каналов образованы отдельными атомами или группами атомов, расположенными по определенному закону. Такие системы характерны для ряда микропористых кристаллических адсорбентов, у которых линейные размеры пор ( каналов) соизмеримы с межатомными расстояниями. Типичным, широко распространенным примером подобных адсорбентов служат цеолиты. Рентгенографические исследования таких систем основаны на методах структурного анализа дифракционной картины при больших углах рассеяния, позволяющих весьма точно локализовать расположение отдельных атомов. Зная соответствующие межатомные или межмолекулярные расстояния, можно определить параметры микропористой структуры. [30]
Страницы: 1 2 3