Изомер - соединение
Cтраница 2
Такие обладающие плоскостью симметрии оптически недеятельные изомеры соединений с несколькими асимметрическими атомами называют мезоизомерами или мезоформами. [16]
На основании фотометрических измерений равновесного распределения двух изомеров соединения 163 в тонкослойных хроматограммах при - 32, - 11, 0 и 15 С была вычислена свободная энтальпия активации AG 20 3 ккал / моль 3 % при 60 С. Эта величина оказалась того же порядка, что и найденная методом ЯМР Кесслером и Рикером [119] для цис-транс-изо-меризации некоторых орго-замещенных ацетанили-дов. Поскольку до настоящего времени разделение было возможно только для амидов, можно предполагать, что отмеченное явление связано не с конформа-ционной, а скорее с с-г / оанс-изомерией замещенных ацетанилидов. [17]
Координационная теория предсказывает существование от одного до трех изомеров соединений двухвалентной платины в зависимости от состава соединения. [18]
Можно было ожидать, что при метилировании Д8 - изомера соединения ( 157) будет образовываться главным образом Д8 - изомер соединения ( 158), поскольку в этом случае отсутствие аксиального атома водорода при С-8 должно облегчить антипараллельную атаку на енолят. В действительности же было получено [224] соответствующее соединение с uc - сочленением колец С и D с высоким выходом. Причина этой аномалии не ясна. Возможно, однако, что 15Р ( а) - водородный атом, будучи сближен с центром С-13 в результате наличия Д8 - связи, столь же эффективно блокирует алкилирование с той же стороны молекулы. [19]
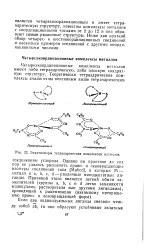 |
Энантиомеры тетраэдрических комплексов металлов. [20] |
Однако на практике до сих пор не удалось расщепить право - и левовращающие изомеры соединений типа [ Mabcd ], в которых М - металл и а, Ь, с, d - различные монодентатные ли-ганды. [21]
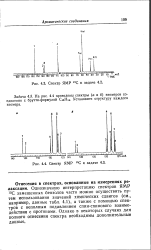 |
Спектр ЯМР 13С к задаче.| Спектр ЯМР 13С к задаче. [22] |
Задача 4.3. На рис. 4.4 приведены спектры ( а и б) изомеров соединения с брутто-формулой CisHu. [23]
 |
Химические сдвиги 13С ( м. д. от ТМС изомеров да 1 3-бутадиенил - 1 халькогенидов. XVI, XXIX, ХХХШ, Э ( С1С2 - СзС4 2 [ 155J. [24] |
В связи с этим в табл. 28, где представлены ХС 13С изомеров соединений XVI, XXIX, XXXIII, некоторые величины обведены штриховой рамкой, означающей, что внутри ее возможно и иное отнесение отдельных сигналов. В случае тел-лурида XXXIII такая линия охватывает значения ХС как цис-транс -, так и / иранс-транс-изомеров, поскольку их содержание в изученных образцах хотя изменялось, но оставалось достаточно близким и интегральные интенсивности соответствующих сигналов были почти одинаковыми. [25]
 |
Химические сдвиги 13С ( м. д. от ТМС изомеров дй ( 1 3-бутадиенил - 1 халькогенидов. XVI, XXIX, XXXIII, Э ( С1С2 - СзС4 2 [ 155J. [26] |
В связи с этим в табл. 28, где представлены ХС 13С изомеров соединений XVI, XXIX, XXXIII, некоторые величины обведены штриховой рамкой, означающей, что внутри ее возможно и иное отнесение отдельных сигналов. В случае тел-лурида XXXIII такая линия охватывает значения ХС как цис-транс -, так и / геранс-транс-иэомеров, поскольку их содержание в изученных образцах хотя изменялось, но оставалось достаточно близким и интегральные интенсивности соответствующих сигналов были почти одинаковыми. [27]
Согласно хромато-масс-спектрометрическому исследованию образец Б состоит из смеси соединений II, IV и изомера соединения III. Это свидетельствует о том, что, во-первых, образующийся на стадии сочетания изомер соединения III может проходить через стадию окисления без изменения. Во-вторых, появляющийся на этой стадии изомер соединения I на стадии окисления способствует образованию соединения IV. К этому можно добавить, что нами был препаративно выделен и с помощью масс-спектрометрии и спектрометра ЯМР идентифицирован только один изомер соединения II со структурой 2 4 -дихлордифенил - сульфона. I и III, то есть последние представляют собой соответствующие 2 4 -дихлорзамещенные соединения. [28]
Согласно хромато-масс-спектрометрическому исследованию образец Б состоит из смеси соединений II, IV и изомера соединения III. Это свидетельствует о том, что, во-первых, образующийся на стадии сочетания изомер соединения III может проходить через стадию окисления без изменения. Во-вторых, появляющийся на этой стадии изомер соединения I на стадии окисления способствует образованию соединения IV. К этому можно добавить, что нами был препаративно выделен и с помощью масс-спектрометрии и спектрометра ЯМР идентифицирован только один изомер соединения II со структурой 2 4 -дихлордифенил-сульфоиа. Поэтому было предположено, что 2 4 - ДХДФС генетически связан с изомерами соединений I и III, то есть последние представляют собой соответствующие 2 4 -дихлорзамещенные соединения. [29]
Обнаружение указанных соединений показывает, что на стадии сочетания, наряду с основным продуктом I, происходит образование изомеров соединений I и III. В то же время можно отметить, что на этой: же стадии происходит полихлорирование образующегося дифенилсуль-фида, что приводит к появлению трихлордифенилсульфида. [30]
Страницы: 1 2 3 4