Изомер - соединение
Cтраница 3
Обнаружение указанных соединений показывает, что на стадии сочетания, наряду с основным продуктом I, происходит образование изомеров соединений I и III. [31]
Можно было ожидать, что при метилировании Д8 - изомера соединения ( 157) будет образовываться главным образом Д8 - изомер соединения ( 158), поскольку в этом случае отсутствие аксиального атома водорода при С-8 должно облегчить антипараллельную атаку на енолят. В действительности же было получено [224] соответствующее соединение с uc - сочленением колец С и D с высоким выходом. Причина этой аномалии не ясна. Возможно, однако, что 15Р ( а) - водородный атом, будучи сближен с центром С-13 в результате наличия Д8 - связи, столь же эффективно блокирует алкилирование с той же стороны молекулы. [32]
Для изомерных форм азотсодержащих соединений Ганч пред ложил обозначения син - и анти -, соответствующие обозначениям цис - и транс-геометрических изомеров соединений, содержащих двойную связь. [33]
Если симметризация происходит с рацемизацией обеих молекул, то независимо от конфигурации молекул исходного вещества, должны образоваться все три возможных изомера конечного симметричного ртутпо-органического соединения. [34]
Однако последняя стадия синтеза - гидрирование 17-кетона ( 427) - протекает в данном случае неселективно, и наряду с 14а - изомером соединения ( 428) ( выход 26 %) образуется в преобладающем количестве ( выход 34 %) неприродный 140-изомер. [35]
В сан - ( Да) - и анти - ( Ц S) - конфигурациях кето-гидразонной формы соединений 1 - 8 я анти - изомере соединения 9 имеются конфор-иации, в когорьк CIN - связь эклиптируют атомы водорода, очевидно, именно в этих нонформациях и будет существовать кето-гидра-зонный таутомер. Отсюда можно сделать заключение, что стабильность кето-гидразонной формы соединений 1 - 9 должна относительно мало зависеть от стерических требований группы R в р-положении. [36]
 |
Пространственный ход пиролиза З - фенил-2 - бутилксантогената. [37] |
Так как в фенониевом ионе А две алкильные группы заслонены, а в В - трансоидны ( рис. 6 - 29), можно ожидать, что зрытро-изомеры соединений II будут сольволизоваться быстрее, чем mpeo - изомеры соединений I и III. Оказалось [40], что сольволиз / npeo - изомера протекает быстрее, чем эритро-изомера лишь в 1 2 раза. Вероятно, фенил принимает участие в реакции только после достижения переходного состояния. [38]
Большинство желтых и оранжевых бензоиламиноантрахинонов активно; таковы, например, Алголевый желтый WG ( 1-бензоилами-ноантрахинон), Индантреновый желтый GK ( 1 5-дибензоил-аминоантрахинон), Парадоновый желтый 5GK ( I) и Индантреновый желтый 5GK, являщийся изомером соединения I и получающийся из изофталевой кислоты. Производные ( 5-аминоантрахинона, по-видимому, более активны, чем а-изомеры; ди - 5-антрахинонилмоче-вина ( Алголевый желтый 4GK; Гелиндоновый желтый 3GN), не применяющийся больше в качестве красителя, являлся наиболее сильным разрушителем волокна в серии красителей, изученной Лан-дольтом. Интересным исключением является Каледоновый желтый 4G ( II), оказавшийся неактивным 77 однако его светопрочность ( 4 - 5) недостаточна для крашения оконных занавесей. [39]
Приставка алло относится к конфигурации замещающих групп при атоме углерода в третьем положении. Изомеры соединений, имеющих два хиральных центра, называются диастереоизомерами. [40]
 |
Структуры L - P1 - [ Cotrien ( am ] 2 [ IMAGE ] - 49. Один изомер ( a H L - pV [ Cotrien ( am ] 2 ( б. хлоротетраэтиленпента. [41] |
В соединении с глицином для й-р 2-изомера был обнаружен только один положительный эффект Коттона, но для / - Pi-соединения наблюдаются две отрицательные полосы. Изомер соединения с саркозином показывает только одну отрицательную полосу КД. Путем сравнения с быс - ( этилендиаминовыми) комплексами / - р2 - саркозина-ту и / - ргглицинату приписана. [42]
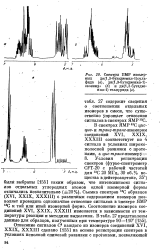 |
Спектры ПМР изомерных ди ( 1 3-бутадиенил - 1 суль-фида ( а, ди ( 1 3-бутадиенил - 1-селеннда ( б н ди ( 1 3-бутадие-нил - 1 теллурида ( в. [43] |
Съемка спектров 13С образцов ( XVI, XXIX, XXXHI) с различным содержанием изомеров позволяет проводить однозначное отнесение сигналов в спектре ЯМР 13С к той или иной изомерной форме. Соотношение изомеров соединений XVI, XXIX, XXXIII изменяется в зависимости от температуры реакции и методики выделения. [44]
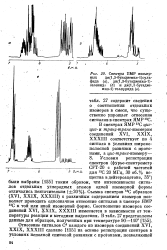 |
Спектры ПМР изомерных ди ( 1 3-бутадиенил - 1 суль-фида ( а, ди ( 1 3-бутадиенил - 1-селеннда ( б н ди ( 1 3-бутадие-нил - 1 телдурида ( в. [45] |
Страницы: 1 2 3 4