Поворотная изомерия
Cтраница 1
Поворотная изомерия дивинил сульфида, - сульфоксида и - сульфона. [1]
Поворотная изомерия и заторможенность внутреннего вращения имеют одну и ту же причину - наличие потенциальных барьеров. На заторможенность внутреннего вращения указывает также факт, что теплоемкость молекул, содержащих единичные С-С - связи, находится между значениями, характерными для вращательных и колебательных степеней свободы. [2]
Поворотная изомерия в эфирной группе полиметилметакрилата и ее проявление в инфракрасных спектрах поглощения, Высокомол. [3]
Поворотная изомерия более эффективно сворачивает цепь в клубок, чем крутильные, а тем более, и валентно-деформационные колебания. [4]
Поворотная изомерия полимеров установлена рядом методов, прежде всего методом инфракрасной спектроскопии. [5]
Обычно поворотную изомерию иллюстрируют на примере этана. Конформаций молекулы этана отличаются положениями метальных групп СН3 друг относительно друга. В остальном этан похож на молекулу водорода: оба радикала СН3 удерживаются одной s - электронной обменной связью ( а-связью), вокруг которой, казалось бы, возможно свободное вращение. Хотя атомы водорода каждого метильного радикала и удалены от атомов водорода партнера, обменное взаимодействие между ними сохраняется, причем, поскольку все связи насыщены, то возникает отталкивание. Поэтому, если считать этан замещенным метаном и соответственно изображать его двумя тетраэдрами с взаимопроникающими вершинами, необходимо предположить, что энергетически выгоднее будет конформация, при которой один тетраэдр повернут вокруг оси С-С на 60 по отношению к другому. [6]
Термин поворотная изомерия предложен впервые И. В. Обреимовым в 1944 г. в беседе с автором этой книги. Ранее в русской научной литературе применялись термины ротационная, или констелляционная, изомерия. [7]
 |
Поворотные изомеры 1 2-ди. [8] |
Изучение поворотной изомерии очень важно с точки зрения определения термодинамических свойств молекул, теории строения макромолекул [197, 198], а также для выяснения вопросов, связанных с механизмом и скоростью реакций. [9]
 |
Поворотные изомеры - бутана. а - транс, 6 ж е - свернутые. [10] |
Существование поворотной изомерии у малых молекул и значение Аи1 ( разности потенциальной энергии у транс - и свернутых изомеров) определяются рядом методов, в частности спектроскопически. [11]
Чувствительность поворотной изомерии к межмолекулярному взаимодействию понятна и естественна. Само явление определяется взаимодействием не связанных друг с другом атомов, имеющим характер ван-дер - Ваальсова взаимодействия. Так как расстояния между этими атомами того же порядка, что и расстояния между соседними молекулами, взаимодействия внутри молекулы, ответственные за поворотную изомерию, не могут существенно отличаться от межмолекулярных. В этом смысле параметры поворотных изомеров ( ДЕ, ср) должны рассматриваться как характеристики жидкости в целом, а не отдельной молекулы. Очевидно, что для уточнения теории, изложенной в настоящем параграфе, необходим учет межмолекулярных взаимодействий высших порядков - квадрупольного, октуполыюго. [12]
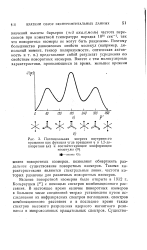 |
Потенциальная энергия внутреннего. [13] |
Явление поворотной изомерии было открыто в 1932 г. Кольраушем [17] с помощью спектров комбинационного рассеяния. В настоящее время наличие поворотных изомеров в большом числе соединений твердо установлено путем исследования их инфракрасных спектров поглощения, спектров комбинационного рассеяния и в последнее время также спектров высокого разрешения ядерного магнитного резонанса и микроволновых вращательных спектров. [14]
Следовательно, поворотная изомерия может осуществляться в любых линейных полимерах. Это положение требует, очевидно, экспериментальной проверки. [15]
Страницы: 1 2 3 4 5