Изопотенциал
Cтраница 1
Изопотенциалы найдены при помощи потенциометрической модели. Линии тока ( пунктирные) между скважинами начертаны перпендикулярно изо-потенциальным линиям. [2]
Изопотенциалы для системы NaNO2 - Na2CO3 - Н2О прямолинейны и по отношению к оси ординат имеют расходящееся расположение с переходом через прямой угол. [3]
 |
Фотография развития процесса вытеснения жидкости из пористой среды вокруг криволинейного барьера в модели элемента пятискважшшого размещения. [4] |
Для размещения линий изопотенциала используются два поисковых электрода. Изопотенциальные линии переносятся на карту изопахит пантографом. [5]
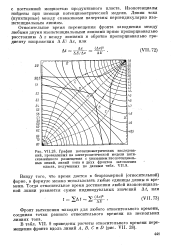
Рассмотрим сначала взаимное расположение изопотенциал трех компонентов. Уравнения изопотенциал целесообразно взять в форме ( 4), так как именно это представление лучше всего отражает взаимную связь химических потенциалов всех компонентов системы. [6]
В определенном смысле понятие изопотенциалы соединения представляет собою обобщение понятия изотермы растворимости соединения постоянного состава. [7]
В частности, отсюда следует, что изопотенциалы любых двух компонентов ни в одной точке треугольника Гиббса не касаются друг друга. [8]
Таким образом, зная направления касательных к изопотенциалам двух компонентов в точке их пересечения, можно для той же точки совершенно однозначно определить направление касательной к изопотенциале 3-го компонента. [9]
В проводимых далее рассуждениях будут использоваться такие формы уравнения изопотенциал, которые позволяют получать необходимые результаты наиболее простым образом. Оказывается, что некоторые результаты получаются особенно легко, если уравнение изопотенциалы выражено в метрике потенциала Гиббса. [10]
Уравнение ( 4) имеет ту особенность, что, являясь уравнением изопотенциалы соединения, оно выражено через изменения химических потенциалов компонентов при ином способе изменения состава раствора, а именно, при изменении состава по обобщенной ноде. Отсюда следует, что закономерности в расположении изопотенциал компонентов и соединений самым тесным образом связаны с закономерностями, характеризующими изменение химических потенциалов компонентов и соединений при некоторых способах изменения состава раствора. [11]
Наиболее простое доказательство этих утверждений может быть дано в том случае, если уравнения изопотенциал выражены в метрике потенциала Гиббса. Согласно вышесказанному, вектор обобщенной ноды х и касательный вектор к изопотенциале соединения V образуют ортогональный базис. Аналогично вектор Xj и вектор, касательный к изопотенциале соединения У, также образуют ортогональный базис. [12]
В определенном смысле аналогичные закономерности характеризуют изменения химических потенциалов компонентов при изменении состава раствора по нодам, а в случае изопотенциал - по обобщенным нодам. [13]
Ответ на сформулированный выше вопрос дает следующее предложение: если фигуративная точка У лежит внутри угла сопряженных диаметров, то касательная к изопотенциале соединения V % проходит вне этого угла ( и наоборот); если точка лежит на одной из сторон угла сопряженных диаметров, то касательная к изопотенциале соединения Kj совпадает с другой стороной угла. [14]
Таким образом, правило об угле сопряженных диаметров позволяет определить взаимное расположение следующих кривых: а) изопо-тенциал двух соединений или компонентов; б) изопотенциалы соединения и изотермы ( изобары) двухфазного равновесия ( изотермы-изобары пара, изотермы растворимости, изотермы расслаивания); в) двух различных изотерм-изобар. [15]
Страницы: 1 2 3