Изотерма - обмен
Cтраница 2
Уравнение изотермы обмена ионов, основанное на законе действия масс, вполне удовлетворительно описывает процесс нонообмена при условии, что процесс обратим и ионная сила обменивающихся ионов как в твердой, так и в жидкой фазе не меняется. [16]
Рассмотрение изотермы обмена ионов, осложненной комплексо-образованием [ т ], показало, однако, что определяемая этим методом величина заряда частиц в системах с комплексообразованием не характеризует среднего заряда частиц, поглощенных ионитом, и тем более среднего заряда частиц в растворе. Воспроизводимость результатов для разных пар смол при этом исключается. Таким образом, этот метод может быть применен только в том случае, когда в системе отсутствует комплексообразование и в фазу смолы переходит только один ион. [17]
Поэтому графически изотерма обмена для такой системы, описывающая, например, сорбцию Се3 как функцию его концентрации, а также как функцию сорбции и концентрации остальных компонентов, может быть изображена в виде гиперповерхности. [18]
 |
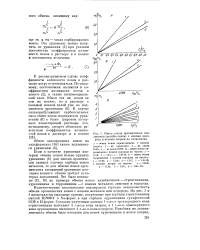
Изотерма иеннвго обмена RH - ( - NH. [19] |
Пунктир - условная изотерма обмена для случая отсутствия селективности. [20]
Сравнение положений изотерм обмена для двух исследованных систем ( рис. 1) показало, что расплавленное стекло ( жидкий обмен-ник) в равновесии с расплавом сульфатов обладает повышенным сродством к тяжелым ионам большего размера ( К и Na), а твердое стекло в равновесии с расплавами нитратов преимущественно поглощает легкий ион малого размера ( Li), причем с повышением температуры селективность поглощения этого иона обменником увеличивается. [21]
Из рассмотренных уравнений изотермы обмена ионов, как указывалось выше, могут быть использованы только уравнения ( 12), ( 13) и ( 15) и лишь при том условии, что процесс ноно-обмена обратим и не осложнен другими явлениями или ж обмен ионов сопровождается побочными процессами, которые можно учесть. [22]
При высоких значениях с изотерма обмена может располагаться ниже диагонали. [23]
На рис. 3 приведены изотермы обмена натрия на кальций и аммоний, лантан и аммоний из смесей солей для цеолита, аморфного алюмосиликата и цеолитсодержащего катализатора. Точки пересечения изотерм, соответствующие одинаковой степени обмена катионов, отвечают разным количественным соотношениям г-экв Меп / г-экв NHf в исходном растворе для цеолита, аморфного алюмосиликата и цеолитсодержащего катализатора. [24]
 |
Изотермы обмена Н - Me на различных образцах. [25] |
Для большинства изученных ионов изотермы обмена Н - Ме имеют S-образный вид, что свидетельствует об обращении селективности катионитов в зависимости от соотношения конкурирующих противоионов в твердой фазе. Преимущественное поглощение ионов металла по сравнению с ионами водорода наблюдается при различных значениях эквивалентной доли ионов Ме в фазе катионита, что зависит от природы сорбируемого иона и типа образца. [26]
 |
Схемы ионообменного умягчения воды на неподвижном слое ( а и в противотоке ( б. [27] |
В зависимости от характера изотермы обмена и от кинетических особенностей процесса ( что отражается на величине ВЭТС) для полной замены одних ионов другими требуется различная высота слоя ионита. Чем большим сродством к извлекаемому иону характеризуется ионит, тем меньшему числу ступеней должна соответствовать высота слоя ионита. [28]
В целом подобный ачализ изотерм обмена на неидеальном ионите не может считаться точным и должен рассматриваться как приближение, так как целиком относит неидеальность ионита за счет его полифункциональности. В тех случаях, когда изотерма обладает резко выраженными особенностями, принципиально не объясняемыми полифункциональностью, такой анализ теряет смысл и часто оказывается невозможным с математической точки зрения. [29]
 |
Обмен ионов органических соединений ( антибиотиков с ионами водорода и ионами натрия на катионитах. [30] |
Страницы: 1 2 3 4 5