Изотерма - обмен
Cтраница 3
Если в качестве уравнения изотермы обмена ионов можно принять уравнение ( 6) для многих практически важных случаев сорбции ионов металлов, то для обмена ионов органических соединений уравнение изотермы ионного обмена требует некоторых дополнений. Это было показано [15, 16] на примере обмена ионов антибиотиков - стрептомицина, ауреомицина и террамицина - с ионами металлов, аммония и водорода. [31]
 |
Углы отражения и относительные интенсивности соответствующих линий для разных катионных форм синтетического фожазита. [32] |
При исследовании кинетики и изотерм обмена Na в цеолите NaY на ионы NH, Ca2, La3, Ce3 установлено [339], что максимальная степень обмена не превышала 70 % и увеличивалась при многократной обработке цеолита раствором соответствующих солей или при повышении температуры процесса. Зафиксировано деформирующее влияние катионов на кристаллическую решетку исходного цеолита. [33]
Равновесная точка лежит на изотерме обмена данной пары ионов и характеризует обменную емкость в момент равновесия. [34]
Точки пересечения на всех изотермах обмена из смесей солей лантана и аммония соответствуют меньшим отношениям концентраций катионов в исходном растворе, чем для смесей кальция и аммония, что еще раз подтверждает большую избирательность дзученных ионобменников к лантану. [35]
Как видно из рисунков, изотермы обмена щелочных катионов на кобальт из обоих исследованных растворов близки для цеолитов одного и того же структурного типа как по характеру и расположению, так и по предельным замещениям. [36]
Для системы I были сняты изотермы обмена ионов лития и калия при 900, 950 и 1000 С, а для обмена лития и натрия - при 950 и 1 - 000 С. Для системы 2 были определены изотермы обмена лития и калия при 400 и 450 С. На рис. 1 приведены некоторые изотермы обмена. [37]
Все расчеты основаны на уравнении изотермы обмена. [38]
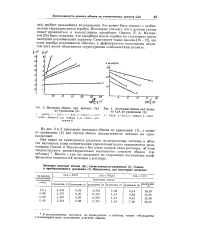 |
Изотермы обмена для цеолита СаА по уравнению ( 2.| Изотермы обмена для цеолита СаА по уравнению ( 1.. T - NAC1. 2 - КС1. 3 - NH. C1. 4 - L1C1. [39] |
На рис. 2 и 3 приведены изотермы обмена по уравнению ( 1), а также по уравнению ( 2) для случая обмена двухвалентного катиона на одновалентный. [40]
Существенно, что в определенных условиях изотерма обмена, представленная в шкале эквивалентных долей, имеет точку перегиба, что соответствует часто наблюдаемым на практике S-образ-ным изотермам. [41]
Высококремнистые цеолиты характеризуются также одинаковым типом изотерм обмена. Так, при обмене Na - Kat они проявляют постоянную селективность к одному иону во всем интервале изменения его концентрации в растворе и цеолите, тогда как при обмене Na - / 2 Kat2 селективность изменяется на обратную при достижении определенной концентрации двухвалентного катиона в твердой фазе. Для исследуемых цеолитов имеют место также идентичные ряды селективности для катионов с близкими свойствами. [42]
Константа обмена определяется тангенсом угла наклона изотермы обмена. [43]
К, приведенные данные позволяют легко построить изотермы обмена соответствующих катионов. Данные, приведенные в табл. 2 и 3, в сочетании с результатами, приведенными в цитированных выше работах, показывают, что особенности внутрицеолптовых растворов проявляются достаточно четко. [44]
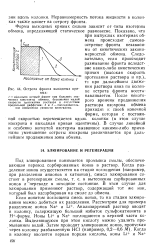 |
Острота фронта выходных кривых. [45] |
Страницы: 1 2 3 4 5