Изотерма - ионный обмен
Cтраница 1
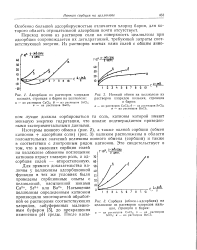 |
Адсорбция из растворов хлоридов кальция, стронция и бария на целлюлозе.| Ионный обмен на целлюлозе из. [1] |
Изотермы ионного обмена ( рис. 2), а также полной сорбции ( обмен катионов адсорбция соли) ( рис. 3) целиком расположены в области положительных значений величины ионного обмена ( сорбции) и также в соответствии с лиотропным рядом катионов. [2]
Изотерма ионного обмена для процесса, в котором участвуют два типа противоионов, может быть получена с использованием электрохимических потенциалов. В процессе переноса ионов при перемещении каждого компонента производится, помимо работы расширения, также и электрическая работа - перенос зарядов. [3]
Изотермы ионного обмена находят широкое применение при расчете емкости сорбции антибиотиков из растворов, в которых заданы концентрации антибиотика и второго конкурирующего иона. Так же может быть оценено влияние изменения состава культура льны х сред на сорбционную емкость антибиотиков, хотя ввиду сложного состава раствора подобная оценка может быть только качественной или в лучшем случае полуколичественной. Характер изотермы ионного обмена, как будет показано далее, играет решающую роль в предсказании наиболее выгодных условий проведения динамических ( колоночных) процессов поглощения и вытеснения антибиотиков. [4]
Изотерма ионного обмена представляет собой кривую зависимости Az от А8 при заданной общей концентрации равновесного раствора и постоянной температуре. [5]
 |
Наиболее распространенные типы адсорбционных колонок. [6] |
Изотерма ионного обмена ( см. рис. 228) в своей линейной печальной части сходна с изотермой адсорбции, но Затем вблизи области насыщения имеется резкий изгиб, после чего кривая переходит в горизонтальную линию. Сильная кривизна изогнутой части кривой объясняет возникновение резко, разграниченных зон при прохождении исследуемого раствора через колонку и проявлении хроматограммы раствбрами электролитов. [7]
 |
Наиболее распространенные типы адсорбционных колонок. [8] |
Изотерма ионного обмена ( см. рис. 228) в своей линейной начальной части сходна с изотермой адсорбции, но затем вблизи области насыщения имеется резкий изгиб, после чего кривая переходит в горизонтальную линию. Сильная кривизна изогнутой части кривой объясняет возникновение резко разграниченных зон при прохождении исследуемого раствора через колонку и проявлении хроматограммы растворами электролитов. [9]
Изотерма ионного обмена выражается ломаной линией, что соответствует быстрому протеканию ионообменной реакции в тех же координатах при постоянной температуре. [10]
Изотерма ионного обмена ( сорбции) характеризует состояние ионообменного равновесия при постоянной температуре. Она связывает между собой количества обменивающихся ионов в каждой из фаз. Изотерма сорбции позволяет судить о селективности ионита, проводить расчеты необходимого числа ступеней ( количества аппаратов), а при расчете размеров колонок ее используют для определения средней движущей силы процесса массообмена. Изотерма сорбции выражается графически или аналитически. Основы теории ионообменного равновесия рассмотрены в гл. [11]
Поэтому изотермы ионного обмена подобны изотермам адсорбции. Они выражаются функцией общего вида а / ( с), где а - концентрация поглощенного вещества ( иона) в сорбенте ( ионите); с - концентрация этого же вещества в растворе при равновесии. [12]
Из изотерм ионного обмена были найдены значения ат и К. [13]
Уравнение изотермы ионного обмена ( 2) отражает закон действующих масс в ионном обмене. [14]
Уравнение изотермы ионного обмена для процесса сорбции диполяр-ных ионов, очевидно, должно отличаться от уравнения обмена ионов с одноименными зарядами. [15]
Страницы: 1 2 3 4 5