Изотерма - ионный обмен
Cтраница 2
Уравнение изотермы ионного обмена было получено рядом ученых. [16]
Обоснованные упрощения изотермы ионного обмена могут быть отнесены прежде всего к фазе раствора. [17]
Вогнутая форма изотермы ионного обмена в области низких концентраций ПАВ в растворе не позволяет повысить степень очистки сточных вод с помощью многоступенчатого ионообменного процесса. Использование активированных углей для до-очистки сточных вод от небольших остаточных концентраций ПАВ позволяет добиться практически полного извлечения ПАВ из сточных вод. Последовательная регенерация углей и аниони-тов водно-метанольными или водно-ацетоновыми растворами хлористого натрия позволяет получать относительно концентрированные регенерационные растворы, из которых выделение чистого растворителя экономически целесообразно. [18]
Входящие в уравнение изотерм ионного обмена константы &i, характеризуют относительную сорбируемость обменивающихся ионов. При этом возможны три случая: / Ci, 1 - г-ый ион сорбируется сильнее, чем первый; kit 1 - оба обменивающихся иона сорбируются одинаково; &1) 4 1 - t - ый ион сорбируется слабее, чем первый. [19]
Три последних уравнения описывают изотерму ионного обмена. [20]
 |
Изобара адсорбции палладием. [21] |
Ионнообменное равновесие характеризуется также изотермой ионного обмена 16 ], которая дает зависимость концентрации растворенного вещества в ионите от концентрации его в растворе. Концентрации обычно выражают в шшлимолях или миллиграмм-эквивалентах на грамм ионита и 1 сма раствора или в эквивалентных, долях. При обмене разновалентяых ионов вид изотермы определяется валентностями обменивающихся жонов. [22]
В литературе приводится несколько уравнений изотермы ионного обмена. [23]
 |
Теоретические кривые распределения иона, сорбируемого в динамических условиях при разных значениях ионного отношения и констант обмена. [24] |
Константа обмена входит в уравнение изотермы ионного обмена и определяет относительную сорбируемость обменивающихся ионов. [25]
В литературе приводится несколько уравнений изотермы ионного обмена. [26]
 |
Изотерма обмена ионов.| Изотерма обмена ионов на Na-катионите ROA. [27] |
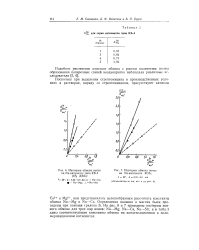
На рис. 6 и 7 приведены изотермы ионного обмена для трех пар ионов: Na-Mg, Na-Са, Na-Str, а в табл. 3 даны соответствующие константы обмена на конденсационном и поли-меризационном катионитах. [28]
Полученное уравнение является наиболее общим выражением изотермы ионного обмена в гетерогенных системах. [29]
В 1926 г. С. М. Липатов вывел уравнение изотермы ионного обмена между адсорбентом и раствором в форме, принятой в настоящее время. [30]
Страницы: 1 2 3 4 5