Изотерма - ионный обмен
Cтраница 3
В литературе приводится целый ряд уравнений изотермы ионного обмена. [31]
Для полифункциональных ионитов приведенные выше уравнения изотермы ионного обмена ( 4), ( 6), ( 8), ( 11) неприменимы. [32]
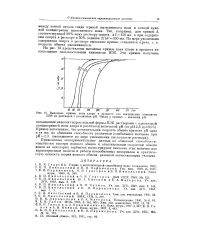 |
Выходные кривые иона хлора в процессе его поглощения анионитом ПЭК из растворов с различным рН. Числа у кривых - значения рН. [33] |
Приведенные экспериментальные данные по обменной способности, константам изотерм ионного обмена и относительным скоростям обмена ионов на некоторых сорбентах иллюстрируют значение этих величин для характеристики свойств и работы ионообменных материалов и практическую ценность теории ионного обмена, развитой отечественными учеными. [34]
В этих случаях большинство исследователей прибегают к нормированию изотерм ионного обмена. После этого обычным способом рассчитывают константу равновесия и свободную энергию реакции обмена. Правильность указанного метода была поставлена под сомнение в недавно опубликованной работе [10], авторы которой показали противоречивость получаемых таким способом значений свободной энергии. Они предложили другой метод нормирования изотерм, позволяющий сравнивать образцы с различной степенью обмена. [35]
Легко видеть, что при / С / 1 изотерма ионного обмена линейна и UV. При / С / 1 изотерма ионного обмена выпуклая, при / С / / 1 изотерма ионообменного равновесия вогнута; при Кц - - оо выпуклая изотерма превращается практически в. [36]
При разработке препаративных ионообменных методов выделения и разделения веществ уравнения изотермы ионного обмена используются для оценки избирательности сорбции и для анализа закономерностей динамики колоночного процесса прежде всего с целью выявления условий образования резких границ зон ионов в рамках равновесной динамики и с учетом кинетики в рамках неравновесной динамики, что позволяет предсказать условия полного насыщения колонки выделяемым веществом, полной десорбции и получения элюата с высокой концентрацией. [37]
 |
Изотерма ионного J. [38] |
Константа ионного обмена равна тангенсу угла наклона прямой, изображающей изотерму ионного обмена, к оси абсцисс. Физический смысл константы ионного обмена заключается в том, что она позволяет дать количественную характеристику способности ионита к обмену с различными ионами из раствора. При этом возможны три случая. [39]
Таким образом, эти два метода дополняют друг друга и могут быть использованы для снятия изотерм ионного обмена и адсорбции. [40]
Вонрос о применимости закона Н. А. Шилова для динамики ионного обмена может быть решен на основании анализа уравнения изотермы ионного обмена и непосредственных расчетов распределения ионов послойным методом. [41]
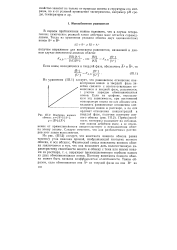 |
Изотерма ионного обмена. х [ В 1 / ГА ]. [42] |
Из рис. (III.2) следует, что константа ионного обмена равна тангенсу угла наклона прямой, изображающей изотерму ионного обмена, к оси абсцисс. Поэтому константа ионного обмена может быть названа коэффициентом селективности. [43]
Мы здесь не будем применять эту систему анализа, так как независимый межфазный перенос воды в рамках анализа изотермы ионного обмена требует рассмотрения переноса десольватированных противоионов, что вызывает определенные затруднения при использовании таких моделей для расчета. Естественно, что разделение воды на приносимую с сольватированными ионами и независимо переносимую воду, сольватирующую матрицу ионитов, при термодинамическом анализе недопустимо. [44]
Для рассмотрения динамики ионного обмена с участием разно-валентных ионов необходимо найти вид динамической изотермы на основе совмещения уравнений изотермы ионного обмена, постоянства обменной емкости и эквивалентного ионного обмена. [45]
Страницы: 1 2 3 4 5