Изотерма - пар
Cтраница 1
Изотермы пара изображают составы газовой фазы с одинаковой температурой конденсации. При температурах выше 60 изотермы весьма мало отличаются от прямых, что свидетельствует об отсутствии ассоциации NH3, CO2 и Н2О в газовой фазе при этих температурах. Эта кривая является границей существования возможных составов газовой фазы. [1]
Изотермой пара называется кривая зависимости давления р пара от его удельного объема v при постоянной температуре. [2]
Изотермой пара называется кривая зависимости давления р пара от его удельного объема v при постоянной температуре. Общий вид изотермы пара изображен на рис. II.5.2. Участок 0 - 1 соответствует ненасыщенному пару, участок 1 - 2 - насыщенному пару и участок 2 - - 3 - жидкости. При дальнейшем уменьшении объема ( участок 1 - 2) давление насыщенного пара не изменяется; часть его переходит в жидкость, и в точке 2 весь пар полностью конденсируется. Уменьшение объема жидкости на участке 2 - 3 требует значительного увеличения давления в связи с малой сжимаемостью жидкостей. [3]
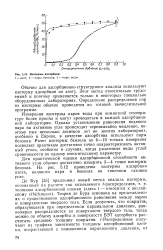 |
Изотермы адсорбции. [4] |
Измерения изотермы паров воды при комнатной температуре более просты и могут проводиться в каждой адсорбционной лаборатории. Однако установление равновесия водяного пара на активном угле происходит черезвычайно медленно, поэтому уже несколько десятков лет во многих лабораториях, особенно в Европе, в качестве адсорбтива используют пары бензола. Рачет изотермы бензола по 6 - 10 точкам измерения позволяет практикам достаточно точно охарактеризовать активный уголь, особенно в случаях, когда различные виды углей сравниваются по одному относительному параметру. [5]
Анализ свыше 200 изотерм инертных паров ( не вызывающих набухания) на различных полимерах позволяет разделить их на те же 4 типа, что и минеральные сорбенты. [6]
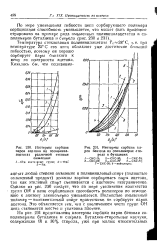 |
Изотермы сорбции ьа-ров бензола на сополимерах стирола и бутадиена. [7] |
На рис. 231 представлены изотермы сорбцшг паров бензола сополимерами бутадиена и стирола. [8]
 |
Сопоставление изотерм адсорбции при 25 С пара ацетона с избыточной адсорбцией ацетона из растворов на силикагеле КСК-25. [9] |
На рис. 1 представлено сравнение изотермы индивидуального пара ацетона [ a / ( p / ps) ] с изотермами избыточной адсорбции ацетона из указанных выше растворов, отнесенных к активности ацетона в объемном растворе. Как видно, в случае адсорбции для системы ацетон-бензол нельзя предполагать существования монослоя. [10]
На рис. 7 - 12 показано несколько изотерм пара, построенных таким образом, начиная с изотермы 145 К. [11]
Подтверждением этого вывода может служить 5-образная форма изотермы паров врды на ртути, которая наблюдается в исключительно чистых условиях проведения опыта [21-23] и указывает на значительное взаимодействие между адсорбированными молекулами воды. [12]
Подтверждением этого вывода может служить - образная форма изотермы паров воды на ртути, которая наблюдается в исключительно чистых условиях проведения опыта [21-23] и указывает на значительное взаимодействие между адсорбированными молекулами воды. [13]
Подтверждением этого вывода может служить - образная форма изотермы паров врды на ртути, которая наблюдается в исключительно чистых условиях проведения опыта [21-23] и указывает на значительное взаимодействие между адсорбированными молекулами воды. [14]
Вывод о термостабильности сделан из величин адсорбции по изотермам паров воды, снятых при температуре 20 С. При температуре 600 С проведены дополнительные опыты по определению термической устойчивости образцов в зависимости от продолжительности прокаливания. [15]
Страницы: 1 2 3