Изотерма - реальный газ
Cтраница 1
Изотермы реального газа ( рис. 2.3, а) отличаются от изотерм идеального газа, которые в координатах р - V изображаются гиперболами. [1]
Изотермы реальных газов, вычисленные по этому уравнению, приблизительно совпадают с опытными данными. [2]
Изотермы реальных газов, построенные по уравнению Ван-дер - Ваальса ( стр. BD, называются перегретой жидкостью. Участок изотермы CF соответствует пересыщенному пару. Участок СЕР практически неосуществим. [3]
Изотермой реального газа называется кривая зависимости молярного объема газа от давления при изотермическом процессе. [4]
Если изотерма реального газа V ( p) известна только в том интервале давлений, для которого на нижнем пределе летучесть не совпадает с давлением fi p, абсолютную величину летучести определить не удается. [5]
Рассмотрим произвольную изотерму реального газа при температуре ниже критической. [6]
Выше t0 изотерма реального газа, начиная от р - О, поднимается кверху, например изотерма EF. [7]
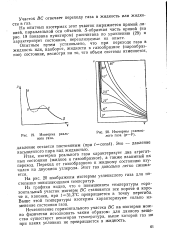 |
Изотерма реального газа.| Изотермы углекислого газа ( р - V. [8] |
Итак, изотерма реального газа характеризует два агрегатных состояния ( жидкое и газообразное), а также взаимный их переход. [9]
Итак, изотерма реального газа характеризует два агрегатных состояния: жидкое и газообразное, а так же взаимный их переход. [10]
При низких температурах изотерма реального газа на диаграмме р, pV имеет минимум, называемый точкой Бойля. [11]
Главной причиной отклонения изотерм реального газа от линии Zl является наличие сил взаимодействия междч молекулами. Модель идеального газа представляет собой систему материальных точек, хаотически движущихся в пространстве и обменивающихся между собой количеством движения при соударениях; в реальном газе между молекулами действуют силы притяжения и силы отталкивания. Силы межмолекулярного взаимодействия имеют электрическую природу, характер их весьма сложен. С увеличением расстояния между молекулами газа силы взаимодействия резко убывают. Поскольку силы притяжения и отталкивания действуют одновременно, результирующая сила FF ( x) равна их алгебраической сумме. [12]
Горизонтальный участок на изотерме реального газа обусловлен процессом превращения газа в жидкость. [13]
При еще более высоких температурах изотермы реального газа минимума не имеют и сжимаемость его при любом давле-нии меньше, чем у идеального газа. [14]
Многочисленные опытные данные показывают, что изотермы реальных газов в приведенных параметрах совпадают только в пределах некоторых классов однотипных веществ, но они существенно отличаются при произвольном подборе веществ, например для спиртов и углеводородов. Это означает, что в общем случае уравнения с тремя постоянными недостаточны для описания свойств реальных газов. [15]
Страницы: 1 2 3 4