Изотерма - реальный газ
Cтраница 3
Из этой картины совершенно очевидно, что с повышением температуры плотность, а следовательно, и давление насыщенного пара увеличиваются ( табл. 3 и 4), как это и было показано при рассмотрении изотерм реального газа. [31]
Этот график представлен кривой а-б-е-г - д-е на рис. 54 и называется изотермой Ван-дер - Ваальса. Изотерма реального газа, полученная опытным путем, изображена на том же рисунке в виде кривой а-б-д-е. Различие двух изотерм состоит в следующем: на изотерме реального газа имеется горизонтальный участок б-д, а изотерма газа Ван-дер - Ваальса имеет форму характерного завитка или волны б-в-г-д в остальном графики двух изотерм практически совпадают. [32]
Это уравнение является основой метода определения летучести. Пусть известна изотерма реального газа 1 - 2 ( рис. 69) до таких давлений ро, когда в пределах погрешности опыта поведения реального и идеального газов заметно не отличаются. Рассмотрим в некотором интервале давлений изотермы v ( p) реального и идеального газов. [33]
Температура, при которой исчезают различия в физических свойствах жидкости и пара, называется критической температурой. Соответствующие критической температуре изотерма реального газа и изотерма газа Ван-дер - Ваальса, называются критическими изотермами. Линия конденсации на критической изотерме реального газа и волнообразный участок на критической изотерме газа Ван-дер - Ваальса вырождаются в точку, которая называется критической точкой. Параметры вещества в критической точке называются критическими параметрами. [34]
Если температура равна критической, линия конденсации изотермы реального газа вырождается в точку и соответственно исчезает, также вырождаясь в точку, характерный завиток на изотерме газа Ван-дер - Ваальса. При температурах, начиная с критической и выше изотермы реального газа и изотермы газа Ван-дер - Ваальса совпадают друг с другом. [35]
При температурах, превосходящих Гкр, но не сильно отличающихся от TKV, изотермы реального газа существенно отличаются от изотерм идеального газа, в особенности в области давлений и объемов, близких к критическим. Однако при температурах, значительно превосходящих 7кр, изотермы реальных газов практически совпадают с изотермами идеального газа. [36]
 |
Иютермы диоксида углерода ii его критическая температура. [37] |
Вернемся теперь к более подробному обсуждению критической точки, которое удобно провести с помощью Р - К-диаграммы, изображенной на рис. 11.12, где показаны пять изотерм, характерных для реального газа, а также одна изотерма для идеального газа. Изотерма идеального газа имеет форму гиперболы, а у изотерм реальных газов наблюдаются значительные отклонения от этой формы, особенно вблизи критической точки. При температурах, несколько превышающих критическую, как, например, Т3 или Т4, газ не поддается сжижению, но при критической температуре Ткрит существует такая точка С на диаграмме, в которой газ находится в равновесии с жидкостью. При более низких температурах, например Т2 или Тъ существует целая область, в которой возможно одновременное существование жидкости и паровой фазы; эта область на рис. 11.12 оставлена светлой, по левую сторону от нее система находится в жидком состоянии. [38]
При р0 любой реальный газ приобретает свойства идеального газа, поэтому изотерма его начинается в той же точке А, что и соответствующая изотерма идеального газа. При низких давлениях, когда объем газа настолько велик, что можно пренебречь влиянием объема самих молекул, действуют только силы взаимного притяжения между молекулами, сжимаемость реального газа по сравнению с идеальным газом увеличивается и изотерма реального газа AN отклоняется вниз. По мере повышения давления второй фактор становится все более существенным, сжимаемость реального газа начинает уменьшаться и изотерма AN отклоняется вверх. Следовательно, изотермы реального газа в pv - р диаграмме имеют минимум. [39]
Для сжижения таких газов их необходимо предварительно охладить, по крайней мере до температуры несколько ниже критической, после чего повышением давления газ может быть переведен в жидкое состояние. Сжиженные таким образом газы удобнее хранить под атмосферным давлением ( в открытом сосуде), но в этом случае их температура должна быть еще более низкой - такой, при которой давление, соответствующее горизонтальному участку изотермы реального газа, равно 1 атм. Для азота такая изотерма соответствует температуре 77 4 К, в то время как критическая температура азота равна 126 1 К. Для кислорода эти цифры соответственно равны 90 К и 154 4 К, для водорода 20 5 К и 33 К и, наконец, для гелия 4 4 К и 5 3 К. Мы упомянули эти четыре газа потому, что именно они широко используются практически: и как средства получения низких температур ( хладоагенты), и для других целей. [40]
Для сжижения таких газов их необходимо предварительно охладить, по крайней мере до температуры несколько ниже критической, после чего повышением давления газ может быть переведен в жидкое состояние. Сжиженные таким образом газы удобнее хранить под атмосферным давлением ( в открытом сосуде), но в этом случае их температура должна быть еще более низкой - такой, при которой давление, соответствующее горизонтальному участку изотермы реального газа, равно 1 атм. Для азота такая изотерма соответствует температуре 77 4 К, в то время как критическая температура азота равна 126 1 К. Для кислорода эти цифры соответственно равны 90 К и 154 4 К, для водорода 20 5 К и 33 К и, наконец, для гелия 4 4 К и 5 3 К. Мы упомянули эти четыре газа потому, что именно они широко используются практически: и как средства получения низких температур ( хладоагенты), и для других целей. [41]
Состояние вещества, при котором исчезают различия в физических свойствах жидкости и пара, называется критическим, температура, соответствующая такому состоянию - критической температурой. Изотерма реального газа и изотерма газа Ван-дер - Ваальса, соответствующие критической температуре, называются критическими изотермами. [42]
 |
Кривая Бойля ( 2. [43] |
График функции zl называется кривой идеального газа. Изотермы реального газа пересекают кривую z при определенных значениях давления. Геометрическое место указанных точек в р, Г - диа-грамме изображает кривую идеального газа. [44]
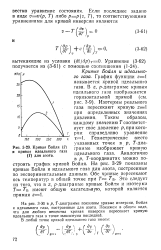
Для исследования поведения реального газа рассмотрим изотермы Ван-дер - Ва-альса - кривые зависимости р от Vm при заданных Т, определяемые уравнением Ван-дер - Ваальса (61.2) для моля газа. Эти кривые ( рассматриваются для четырех различных температур; рис. 89) имеют довольно своеобразный характер. При высоких температурах ( ТТк) изотерма реального газа отличается от изотермы идеального газа только некоторым искажением ее формы, оставаясь монотонно спадающей кривой. При некоторой температуре Гк на изотерме имеется лишь одна точка перегиба К. Эта изотерма называется критической, соответствующая ей температура 7 к - критической температурой. Критическая изотерма имеет лишь одну точку перегиба К, называемую критической точкой; в этой точке касательная к ней параллельна оси абсцисс. Соответствующие этой точке объем VK и давление рк называются также критическими. Состояние с критическими параметрами ( рк, VK, TK) называется критическим состоянием. [45]
Страницы: 1 2 3 4