Изотерма - реальный газ
Cтраница 4
Для исследования поведения реального газа рассмотрим изотермы Ван-дер - Ваальса - кривые зависимости р от Vm при заданных Т, определяемые уравнением Ван-дер - Ваальса (61.2) для моля газа. Эти кривые ( рассматриваются для четырех различных температур; рис. 89) имеют довольно своеобразный характер. При высоких температурах ( ТТК) изотерма реального газа отличается от изотермы идеального газа только некоторым искажением ее формы, оставаясь монотонно спадающей кривой. При некоторой температуре Тк на изотерме имеется лишь одна точка перегиба / С - Эта изотерма называется критической, соответствующая ей температура Г к - критической температурой. Критическая изотерма имеет лишь одну точку перегиба К, называемую критической точкой; в этой точке касательная к ней параллельна оси абсцисс. Соответствующие этой точке объем VK и давление рк называются также критическими. Состояние с критическими параметрами ( рк, VK, TK) называется критическим состоянием. [46]
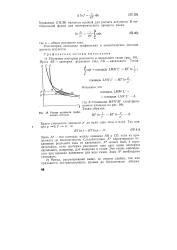 |
Расчет летучести графическим методом. [47] |
Следовательно, Л характеризует отклонение реального газа от идеального. А может быть и отрицательным, если изотерма реального газа идет выше изотермы идеального, например, для водорода и гелия. Это также наблюдается при высоких давлениях для всех газов. [48]
Этот график представлен кривой а-б-е-г - д-е на рис. 54 и называется изотермой Ван-дер - Ваальса. Изотерма реального газа, полученная опытным путем, изображена на том же рисунке в виде кривой а-б-д-е. Различие двух изотерм состоит в следующем: на изотерме реального газа имеется горизонтальный участок б-д, а изотерма газа Ван-дер - Ваальса имеет форму характерного завитка или волны б-в-г-д в остальном графики двух изотерм практически совпадают. [49]
Около точки а изотермы abcdefg вещество имеет свойства газа ( перегретого пара), а около точки g - свойства капельной жидкости. Однако превращение газа в жидкость по уравнению Ван-дер - Ваальса происходит непрерывно, без наступления кризисных явлений в виде появления в определенный момент капелек жидкости; а в дальнейшем полного исчезновения газовой фазы. Эти кризисные явления наступают на пограничных кривых, где изотермы реального газа имеют перелом, в то время как на изотермах Ван-дер - Ваальса такого перелома нет. На участках ab и fg экспериментальная изотерма относительно хорошо согласуется с изотермой Ван-дер - Ваальса, но между точками b и / они резко отличаются друг от друга. [50]
Страницы: 1 2 3 4