Изотерма - идеальный газ
Cтраница 2
На рис. 2 приведены две изотермы идеального газа при 0 и 100 С. Там же показаны экспериментальные ( реальные) изотермы для азота. [16]
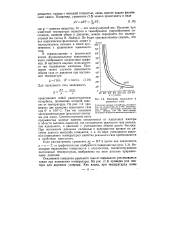 |
Изотермы идеального и реального газа. [17] |
На рис. 1.2 приведены две изотермы идеального газа при 0 и 100 С. Там же показаны экспериментальные ( реальные) изотермы для азота. [18]
Из уравнения Клапейрона следует, что изотермы идеального газа в pv, р-диаграм-ме являются горизонтальными прямыми. [19]
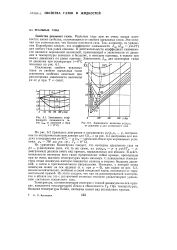 |
Зависимость коэффициента сжимаемости газов 2СЖ от давления р ( при t 0е С.| Зависимость величины pv / p0vQ от давления р для углекислого газа. [20] |
Из уравнения Клапейрона следует, что изотермы идеального газа на pv - р-диаграмме ( или, что то же самое, на pvlpuv0 - р - и pv / RT0 - р-диаграммах) должны иметь вид прямых, параллельных оси абсцисс. В действительности изотермы всех газов представляют собой кривые, проходящие при не очень высоких температурах через минимум. С повышением температуры точки минимума изотерм смещаются сначала в сторону больших давлений, а затем в противоположном направлении. Из этого следует, что как на рассматриваемой изотерме, так и вблизи нее газ с достаточной степенью точности удовлетворяет уравнению состояния идеального газа. [21]
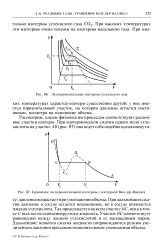 |
Экспериментальные изотермы углекислого газа.| Сравнение экспериментальной изотермы с изотермой Ван-дер - Ваальса. [22] |
При высоких температурах эти изотермы очень похожи на изотермы идеального газа. [23]
Последнее легко представить, имея в виду, что изотерма идеального газа - равносторонняя гипербола. [24]
Таким образом, каждому состоянию, характеризуемому точкой на изотерме идеального газа, соответствует одно и то же значение внутренней энергии идеального газа. [25]
Одним из проявлений этих свойств реальных газов является различное протекание изотерм реальных и идеальных газов в диаграммах состояния, в частности в v - p и p - pv - диаграммах. [26]
Одним из проявлений этих свойств реальных газов является различное протекание изотерм реальных и идеальных газов в диаграммах состояния, в частности в v - p и p - pv - диаграммах. [27]
Изотермы реального газа ( рис. 2.3, а) отличаются от изотерм идеального газа, которые в координатах р - V изображаются гиперболами. [28]
С возрастанием температуры выше критической изотермы постепенно принимают вид плавных кривых, напоминающих изотермы идеального газа. [29]
Отсюда, в частности, видно, что при определенных значениях Л две изотермы идеального газа в 8, А-диаграмме пересекутся. [30]
Страницы: 1 2 3 4