Изотерма - идеальный газ
Cтраница 4
В области, лежащей выше критической изотермы и правее кривой ВК, двухфазное состояние невозможно, и с ростом температуры и объема изотермы приближаются по форме к изотермам идеального газа PV const. [46]
Измеряя давление и объемы газов в большом интервале температур и изображая их изотермы графически, заметим, что изотермы реальных газов при низких температурах и при высоких давлениях будут отличаться от изотермы идеального газа. [47]
По мере того как температура приближается к значению, примерно равному 2 5-кратной критической температуре, точка пересечения имеет место при все более и более низком давлении, пока температура не достигнет такого значения, при котором pv-mo - терма реального газа полностью лежит выше изотермы идеального газа. Эта температура, выше которой объем реального газа всегда больше, чем объем идеального газа даже при очень низких давлениях ( в пределе р 0), известна как точка Бойля. [48]
Если учесть, что изотерма и изоэнтальпа ( I const) идеального-газа совпадают и изображаются в координатах is прямой, параллельной оси абсцисс, то станет ясно, что по мере удаления изотермы от пограничной кривой ( увеличение степени перегрева) она все ближе подходит к изотерме идеального газа. [49]
Если учесть, что изотермы и изоэнтальпы ( i const) идеального газа совпадают и изображаются в координатах i - прямой линией параллельной оси абсцисс, то станет ясно, что по мере удаления изотермы от пограничной кривой ( увеличение степени перегрева) она все ближе подходит к изотерме идеального газа. [50]
 |
Иютермы диоксида углерода ii его критическая температура. [51] |
Вернемся теперь к более подробному обсуждению критической точки, которое удобно провести с помощью Р - К-диаграммы, изображенной на рис. 11.12, где показаны пять изотерм, характерных для реального газа, а также одна изотерма для идеального газа. Изотерма идеального газа имеет форму гиперболы, а у изотерм реальных газов наблюдаются значительные отклонения от этой формы, особенно вблизи критической точки. При температурах, несколько превышающих критическую, как, например, Т3 или Т4, газ не поддается сжижению, но при критической температуре Ткрит существует такая точка С на диаграмме, в которой газ находится в равновесии с жидкостью. При более низких температурах, например Т2 или Тъ существует целая область, в которой возможно одновременное существование жидкости и паровой фазы; эта область на рис. 11.12 оставлена светлой, по левую сторону от нее система находится в жидком состоянии. [52]
 |
Плотности жидкого и парообразного эфира ( Юнг, 1910. [53] |
На рис. 43 нанесены изотермы по этому уравнению. В отличие от изотерм идеального газа ( рис. 31), они представляются сложными кривыми с двойным изгибом. [54]
Рассмотрим, как можно найти работу газа при изотермическом процессе. На рис. 5.6 изображена изотерма идеального газа. При таком процессе газ выполняет работу, так как &V в этом случае отлично от нуля. Формулу (5.25) здесь применять нельзя, так как она верна при постоянном давлении р, а в изотермическом процессе р изменяется. [55]
Выясним, как найти работу газа при изотермическом процессе. На рис. 5.6 изображена изотерма идеального газа. При таком процессе газ выполняет работу, так как ДУ в этом случае отлично от нуля. Формулу (5.25) здесь применять нельзя, так как она верна при постоянном давлении р а в изотермическом процессе р изменяется. [56]
 |
Изотермы а. [57] |
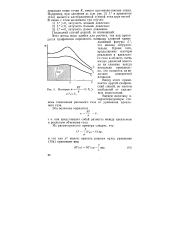
Этот метод мало удобен для расчета, так как приходится графически определять площадь сложной криволинейной фигуры L, что весьма затруднительно. Кроме того, продолжение изотерм реального и идеального газа в область очень малых давлений вплоть до их слияния всегда несколько произвольно, что скажется на величине измеряемой площади. [58]
На рис. 19 представлены три типичные ри-изотермы реального газа для температуры выше критической, равной критической и для температуры ниже критической. Для сравнения приведена pv - изотерма идеального газа для той же температуры выше критической, что и для реального газа. При давлении, большем - - ЛО-кратного критического давления, изотерма реального газа пересекает изотерму идеального газа и объем реального газа становится больше, чем объем идеального газа при тех же температуре и давлении. [59]
Страницы: 1 2 3 4