Изотерма - идеальный газ
Cтраница 3
Таким образом, изотермы Ван-дер - Ваальса не только более точно, чем изотерма идеального газа, передают поведение газа, но охватывают собою и процесс ожижения газов, а также выражают то свойство жидкости, которое проявляется в ее малой сжимаемости. [31]
С возрастанием температуры выше критической, изотермы постепенно принимают вид плавных кривых, напоминающих изотермы идеального газа. [32]
При более высоких температурах ( Т Ткр) изотермы реального газа приближаются к изотермам идеального газа, а участок изотермы с двухфазным состоянием отсутствует. [33]
В любой точке изотермического процесса, совершаемого идеальным газом, выполняется условие pv const, т.е. изотермы идеального газа в р, у-диа-грамме - гиперболы, а в р, - диаграмме ( р - плотность) - прямые линии, идущие из начала координат. [34]
Изотермическое сжатие реального газа при температуре Т % ( TzTK) происходит в соответствии с уравнением изотермы идеального газа лишь до давления, равного давлению насыщенного пара РО при данной температуре Тч. При дальнейшем уменьшении объема часть газа превращается в жидкость, а давление остается постоянным и равным давлению насыщенного пара. [35]
В области перегретого пара после пересечения пограничной кривой х 1 изотерма имеет вид гиперболы, которая положе изотермы идеального газа. [36]
 |
Изотермы идеального газа. [37] |
Зависимость V от р можно представить графически в виде кривых ( рис. 1), которые называют изотермами идеального газа. [38]
Изотермы реальных веществ при температурах ниже критической имеют прямолинейный участок, соответствующий превращению газа в жидкость, тогда как изотермы идеального газа представляют собой разнобокие гиперболы, нигде не имеющие прямолинейного участка. [39]
При температурах, превосходящих Гкр, но не сильно отличающихся от TKV, изотермы реального газа существенно отличаются от изотерм идеального газа, в особенности в области давлений и объемов, близких к критическим. Однако при температурах, значительно превосходящих 7кр, изотермы реальных газов практически совпадают с изотермами идеального газа. [40]
На графике ( рис. 36) видно, что изотерма СО2 при 80 С и 60 С близка к изотерме идеального газа. Начиная с 40 С изотерма СО2 отклоняется от изотермы идеального газа к оси ординат р и далее идет почти параллельно ей. Это указывает на то, что при больших давлениях объем газа почти не меняется с увеличением давления. [41]
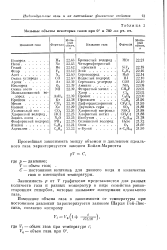 |
Мольные объемы некоторых газов при 0 и 760 мм рт. ст. [42] |
Зависимость р от V графически представляется для разных количеств газа и разных температур в виде семейства равносторонних гипербол, которые называют изотермами идеального газа. [43]
Положительная сторона применения остаточного объема видна из экспериментального наблюдения того, что при низких давлениях ( обычно 1 атм и ниже) изотерма идеального газа приближается к изотерме реального газа таким образом, что а остается конечной и по существу постоянной величиной. [44]
Зависимость р от V для разных температур может быть представлена графически в виде семейства кривых ( равносторонних гипербол), которые называют изотермами идеального газа. [45]
Страницы: 1 2 3 4