Экспериментальная изотерма - адсорбция
Cтраница 2
 |
Изотермы адсорбции, соответствующие уравнению состоят двумерной адсорбированной фазы типа уравнения Ван-дер - Ваальса. [16] |
Приведенные уравнения довольно хорошо описывают отдельные экспериментальные изотермы адсорбции в субмонослойной области. [17]
Для определения константы Генри из экспериментальной изотермы адсорбции, измеренной статическим методом, надо привлечь ту или иную модель состояния адсорбированного вещества, которая позволяет выразить уравнение изотермы адсорбции в аналитической форме, в частности в виде степенного ряда ( вириальные разложения по степеням Г или с), в котором первый член содержит только константу Генри. Этот метод рассмотрен в разд. [18]
В, которые определяются по экспериментальной изотерме адсорбции стандартного пара - бензола. [20]
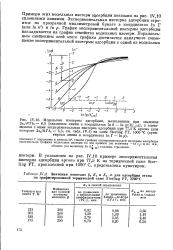
На рис. I, 2 представлены экспериментальные изотермы адсорбции н-парафинов от н - Cg до н - Cjg при 400 С, полученные для стабилизированных образцов. [21]
 |
Константы ш0 и В уравнения адсорбции для изученных цеолитов. [22] |
Жуковой и Н. В. Кельцевым была проведена обработка многочисленных экспериментальных изотерм адсорбции паров и газов для различных температур на гранулированных цеолитах. [23]
Для практических расчетов адсорбционных процессов на экспериментальных изотермах адсорбции индитштгуяд ннт компонентов можно выделить сравнительно небольшие участки, соответствующие по упругостям паров адсорбата условиям работы конкретных аппаратов, и для этих участков изотерм вычислить коэффициенты уравнения Лен-гыюра, которые затем использовать для уравнения Маркгема-Бентона. Задачей настоящего исследования является экспериментальное обоснование такого подхода применительно к рассматриваемой системе. [24]
Уравнение ( FV5) обычно хорошо описывает экспериментальные изотермы адсорбции при малых и средних заполнениях поверхности. [25]
 |
Значения предельных объемов. [26] |
Теория объемного заполнения микропор позволяет по одной экспериментальной изотерме адсорбции, измеренной при некоторой температуре или по одной изобаре адсорбции рассчитать изотермы этого же вещества для других температур. Проведенные различными авторами исследования по адсорбции веществ на микропористых углеродных адсорбентах в рамках ТОЗМ давали хорошее совпадение расчетных и экспериментальных данных, когда предельный объем адсорбционного пространства, оцененный по бензолу, распространялся на вещества, молекулы которых близки по размерам молекулам стандартного вещества. [27]
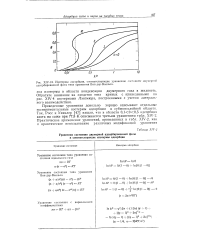
В указанном на рис. IV, 10 примере экспериментальная изотерма адсорбции аргона при 77 5 К на термической саже Sterling FT, прокаленной при 1000 С, представлена пунктиром. [29]
Примеры такого определения констант С1 и С2 из экспериментальных изотерм адсорбции приведены на рис. IV2. Значения Ci практически не зависят от величин интервалов Г или ns, введенных в расчет, и от числа членов в экспоненте уравнения ( IV5), которое менялось от трех до шести. [30]
Страницы: 1 2 3 4 5