Другая изотерма
Cтраница 2
Уже после окончания Международного симпозиума по термометрии были получены данные для четырех других изотерм Не3, которые в виде разности Г48 - Т приведены на фиг. [16]
В ряде случаев лучше согласуются с опытом данные, полученные при использовании других изотерм адсорбции. [17]
Проверка теории состоит из двух стадий: вычисление характеристической кривой из экспериментальной изотермы и вычисление других изотерм по характеристической кривой. Изотерма, применяемая для определения характеристической кривой, должна покрывать распределение потенциала во всем адсорбционном пространстве. Так как участки с низкими значениями потенциала заполняются только при низких температурах, то для вычисления следует пользоваться изотермой для температуры ниже критической. С другой стороны, температура, при которой измерена изотерма, не должна быть слишком низкой, так как в этом случае большая часть адсорбционного пространства заполняется при очень низких давлениях и область высоких потенциалов не может быть оценена с достаточной степенью точности. Если подобная идеальная изотерма не может быть получена практически, то характеристическая кривая должна быть вычислена из двух или более изотерм. [18]
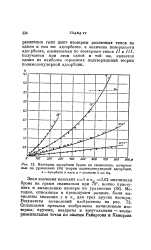 |
Изотермы адсорбции брома на силикагеле, начерченные по уравнению ( 38 теории полимолекулярной адсорбции. - адсорбция в мм / г. р - давление в мм Hg. [19] |
Методом, описанным в предыдущем разделе, были вычислены значения с и vm для трех других изотерм. [20]
Проверка теории состоит из двух стадий: вычисление характеристической кривой из экспериментальной изотермы и вычисление других изотерм по характеристической кривой. Изотерма, применяемая для определения характеристической кривой, должна покрывать распределение потенциала во всем адсорбционном пространстве. Так как участки с низкими значениями потенциала заполняются только при низких температурах, то для вычисления следует пользоваться изотермой для температуры ниже критической. С другой стороны, температура, при которой измерена изотерма, не должна быть слишком низкой, так как в этом случае большая часть адсорбционного пространства заполняется при очень низких давлениях и область высоких потенциалов не может быть оценена с достаточной степенью точности. Если подобная идеальная изотерма не может быть получена практически, то характеристическая кривая должна быть вычислена из двух или более изотерм. [21]
 |
Изотермы адсорбции брома на силикагеле, начерченные по уравнению ( 38 теории полимолекулярной адсорбция. - адсорбция в лш / г. р - давление в мм Hg. [22] |
Методом, описанным в предыдущем разделе, были вычислены значения с и vm для трех других изотерм. [23]
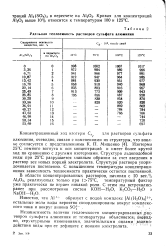 |
Удельная теплоемкость растворов сульфата алюминия. [24] |
Изотерма 25 С немного вогнута к оси концентраций и имеет более крутой ход по сравнению с другими изотермами. Структура льдоподобной воды при 25 С разрушается главным образом за счет введения в раствор все новых порций электролита. Структура раствора упорядочивается постепенно. С повышением температуры концентрационная зависимость теплоемкости практически остается постоянной. [25]
Действительно, изотерма адсорбции паров метанола образцом силикагеля ШСМ, который подвергали гидротермальной обработке при постоянной температуре ( первый опыт), расположена выше других изотерм, ибо в этом случае произошло только одно колебание температуры - при нагреве и охлаждении. Ниже расположена изотерма адсорбции, снятая на таком же образце силикагеля, но подвергнутого гидротермальной обработке при периодических колебаниях температуры, хотя средняя температура опыта была ниже, чем в первом опыте. Еще ниже расположена изотерма адсорбции, снятая на аналогичном образце силикагеля, подвергнутого гидротермальной обработке в условиях кипения. [26]
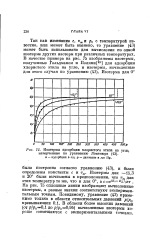 |
Изотермы адсорбции хлористого этила на углэ. [27] |
Так как изменение с, vm и рй с температурой известно, или может быть оценено, то уравнение ( 43) может быть использовано для вычисления по одной изотерме других изотерм при различных температурах. [28]
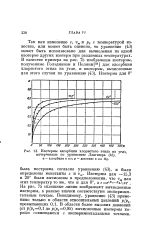 |
Изотермы адсорбции хлористого этила на угла. [29] |
Так как изменение с, vm и р0 с температурой известно, или может быть оценено, то уравнение ( 43) может быть использовано для вычисления по одной изотерме других изотерм при различных температурах. [30]
Страницы: 1 2 3 4