Другая изотерма
Cтраница 3
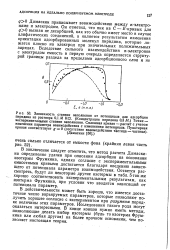
Очевидно, что для некоторых изотерм, представленных на рис. 2, выбор этой точки может решаться непосредственно на основании чертежа ( если изотермы пересекаются с осью ординат при р / р0 1 почти под прямым углом); в отношении же других изотерм необходимо определение десорбцион-ной ветви. Благодаря адсорбционным силам плотность жидкого азота в очень малых порах, повидимому, отличается от обычной плотности жидкости, величину которой используют при расчетах объема пор. Таким образом, применение описанного метода вносит в упомянутые расчеты неопределенность. [31]
В то же время эти опыты показывают, что при изученных температурах аммиачные растворы не: следуют закону Генри-Дальтона. По сравнению с другими изотермами изотерма 60 отличается меньшей кривизной. Однако и при 60 уклонение от упомянутого закона выражено вполне ясно, что видно и из следующего расчета. [32]
Так же построены и другие изотермы. [33]
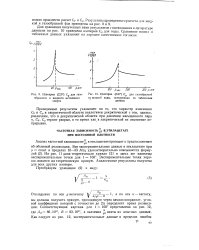 |
Изотерма ( 220 Ср для газообразного и жидкого метилового спирта.| Изотерма ( 340 Ср для газообразной. [34] |
Экспериментальные точки хорошо ложатся на теоретическую кривую. Аналогичные результаты получены для всех других изотерм. [35]
В заключение следует отметить, что метод расчета Дамаски-на определенно удачен при описании адсорбции на основании изотермы Фрумкина, однако согласие с экспериментальными емкостными кривыми достигается благодаря введению завися1 - щего от потенциала параметра взаимодействия. Остается рассмотреть, будут ли некоторые другие изотермы в табл. 5 так же хорошо соответствовать экспериментальным результатам, как изотерма Фрумкина, при условии что вводится зависящий от потенциала параметр. [37]
Это уравнение нельзя назвать полностью приведенным, так как а зависит от ацентрического коэффициента. При Тг 1 изотерма не зависит от и, но другие изотермы в значительной степени связаны с этим коэффициентом, особенно при температурах ниже критической. При ш 0 уравнения Соава и Пенга - Робинсона практически совпадают в масштабе представленного здесь графика. [38]
Поскольку весь интервал данных не может быть полностью описан нв уравнением Фрейндлиха, ни уравнением Ленгмюра, пытались использовать то уравнение, которое более соответствовало оцениваемой части экспериментальных данных. Если последние не могли быть описаны ни той, ни другой изотермой, данные сравнивались без помощи уравнений. [39]
Это уравнение нельзя назвать полностью приведенным, так как а зависит от ацентрического коэффициента. При Т, 1 изотерма не зависит от w, но другие изотермы в значительной степени связаны с этим коэффициентом, особенно при температурах ниже критической. При ш 0 уравнения Соава и Пенга - Робинсона практически совпадают в масштабе представленного здесь графика. [40]
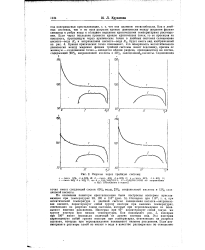 |
Разрезы через тройную систему. [41] |
Изотерма при 90 характеризует собой такую же группу изотерм при низких температурах. Как показывает рис. 5, изотерма при 100 имеет несколько отличный от других изотерм вид. Эта изотерма характеризует собой группу изотерм при температурах, отвечающих на разрезах составам, которые при переохлаждении показывают явление расслоения. [42]
В кинетических уравнениях поверхностную концентрацию адсорбированных частиц часто заменяют их объемной концентрацией, что допустимо в случае незначительных степеней заполнения поверхности электрода реагирующими частицами, когда справедлива изотерма адсорбции 1 енри. Однако коэффициент адсорбции в изотерме Генри, равно как и в случае других изотерм адсорбции, может изменяться с потенциалом электрода. [43]
Это означает, что потенциальная кривая не зависит от температуры и может быть использована для расчета других изотерм. [44]
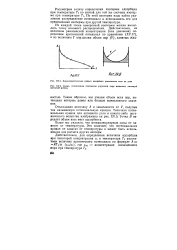 |
Характеристическая кривая адсорбции углекислого газа на угле.| Схема, поясняющая понижение упругости пара жидкости, имеющей вогнутый мениск. [45] |
Страницы: 1 2 3 4