Изотиазола
Cтраница 2
Аналогично рассмотренному выше протекает протонный обмен в метильных заместителях изотиазола: метильные группы в положении 5 депротонируются быстрее, чем в положении 3, а в 4-ме-тильной группе обмен практически не происходит. [16]
Изопропанол 129 Изопропенил 124 Изопропил 123 Изоселеноцианат 139 Изоселеноцианато - 139 Изотиазол 116 Изотиоцианат 139 Изотиоцианато - 139 Изотопно-модифицированные соединения 200 ел. [17]
Изучены пестицидные свойства большого числа производных гиазола [50-74], бензтиазола [75-82], изотиазола [41-45], бензизотиазола [46-49], парабановой и тиопарабановой кислот [83-86], гидантоина и тиогидантоина [87-90] и их производных. [18]
Хотя не было проведено сопоставления относительной легкости электрофильного замещения 1 2-азолов, на основании экспериментальных данных можно заключить, что реакционная способность уменьшается в ряду: пиразол изотиазол изоксазол. Следует отметить, что в этом ряду атака электрофильным агентом осуществляется в положение 4, так как при этом реализуется относительно более устойчивое переходное состояние. [19]
Существуют общие, а также уникальные методы синтеза некоторых особых 1 2-азолов, не пригодные для получения других пиразолов, изотиазолов и изоксазолов: ни реакция пропена с диоксидом серы и аммиаком при 350 С, которая дает незамещенный изотиазол [88] с выходом 65 %, ни синтез [89] из пропаргилового альдегида и тиосульфата ( схема приведена ниже) неприменимы [ прямого синтеза других 1 2-азолов. [20]
Связь S-N имеет двойственную природу: электрофильная атака может происходить по атому азота, нуклеофильная - по атому серы. Изотиазол почти полностью протонируется сильными кислотами, а при обработке смесью концентрированных азотной и серной кислот с высоким выходом получается 4-нитро-изотиазол. В случае 3 - или 5-алкил -, 5-бром -, 5-ацетамидоизотиазо-лов соответствующие продукты нитрования также получаются с высокими выходами. Следует отметить, что 3-фенилизотиазол нитруется в лгега-положение бензольного кольца, а 4-фенилизотиазол дает о - и n - нитрофенилизотиазолы. Галогенирование протекает в разных условиях, однако, например, при бромировании 4-бромпро-изводные получаются с низкими выходами из-за образования комплекса пербромизотиазола. Электронодонориые заместители в положении 3 или 5 ( амино -, гидрокси - или алкоксигруппы) облегчают галогенирование в положение 4, хотя и 3-метилизотиазолкарбоно-вая - 5 кислота ( 253) дает 4-галогенпроизводное с высоким выходом. [21]
Некоторые нуклеофильные реагенты могут расщеплять циклическую систему изотиазолов, бензизотиазолов и их кватернизован-ных производных. Такие заместители в положении 5 изотиазола, как галогены, легко подвергаются нуклеофильному замещению [63, 123, 124, 126] при действии цианидов, гидроксидов, алкоксндов и ряда родственных нуклеофилов. [22]
Изучение химии изоксазола берет свое начало в прошлом веке, тогда как первые упоминания о моноциклических изотиазолах датированы только 1950-ми годами. [23]
По силе действия они превосходят все другие изученные гетероциклические соединения - рядов оксазо-ла, изоксазола, тиазола, изотиазола и фуразана. [24]
По силе действия они превосходят все другие изученные гетероциклические соединения - рядов оксазо-ла, изоксазола, тиазола, изотиазола и фуразана. [25]
Подобно имидазолу пиразол - единственный из этих трех соединений, представляющий собой твердое вещество при комнатной температуре, - имеет высокую температуру кипения ( 187 С), причем гораздо выше, у изотиазола и изоксазола ( 114 и 95 С соответственно); это обусловлено: чием межмолекулярных водородных связей, присущих только пиразолу. Такие ассоциации, по-видимому, принимают формы димеров, гримеров и олигоме-ров; без сомнения, имидазол не способен образовывать димеры. Каждый из 1 2-азолов имеет запах, подобный пиридиновому, но лишь частично растворим в воде. Дигидро - и тетрагидрогетероциклы носят названия пиразолин / пиразо-лидин, изотиазолин / изотиазолидин и изоксазолин / изоксазолидин. Быстрая таутомерия, заключающаяся в перемещении атома водорода от одного атома азота к другому, так же как и в имидазоле, означает, что замещенные пиразолы неизбежно представляют собой смеси, и номенклатура этих соединений аналогична той, которая применяется для имидазолов. [26]
Как правило, гетероциклические соединения группы азолов, с одной стороны, более устойчивы, чем соединения группы фурана, пиррола и тиофена ( например, в кислой среде), но, с другой стороны, менее реакционноспособны, чем соответствующие производные гетероциклов с одним гетероатомом. Следует отметить, что встречаются большие различия в реакционной способности азолов. Например, изотиазол в отличие от тиазола устойчив к окислению перманганатом калия. [27]
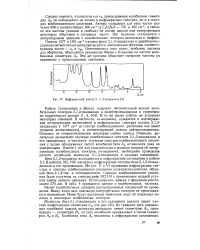 |
Инфракрасный спектр 2, 1, 3-тиадиазола. [28] |
Следует отметить, что частоты v7 и v8, приписываемые колебаниям симметрии Az, не наблюдались не только в инфракрасных спектрах, но и в спектрах комбинационного рассеяния. Авторы указывают для этих частот значения 908 и соответственно 500 см 1 ( у C2D2N2S - 735 и 450 слГ1; в таблице эти частоты указаны в скобках) на основе данной ими интерпретации некоторых обертонов и составных частот. Эти значения согласуются с литературными данными о колебательных спектрах изотиазола и тиофена. [29]
В отличие от азиринов трехчленные циклические азометины, содержащие два гетероатома [ диазирины ( 3046), оксазирины ( 304в) и тиазирины ( 304г), неизвестны. Предполагают, что диазирины и тиазирины могут участвовать как неустойчивые промежуточные соединения в фотохимически индуцированных реакциях 1 3-дипо-лярного циклоприсоедчнения, в которые вступают некоторые ме-зоионные гетероциклы. Так, возможно, что образование производных пиразола ( 327а) и изотиазола ( 3276) при фотолизе сиднонов ( 324а) и их тиаанологов ( 3246) в присутствии диметилового эфира ацетйлендикарбоновой кислоты ( ДМАД) происходит по уравнению ПО. [30]
Страницы: 1 2 3