Установление - ионообменное равновесие
Cтраница 1
Установление ионообменного равновесия - л скорость обмена между двумя фазами связаны с природой имштов, хроматографируе-мых веществ и техникой эксперимента. [1]
Установление ионообменного равновесия и скорости обмена между двумя фазами связаны с природой ионитов, хромато-графируемых веществ и техникой эксперимента. [2]
Скорость установления ионообменного равновесия зависит от ряда внешних и внутренних факторов. Первые в основном зависят от гидродинамического режима жидкости, содержащей обменивающиеся ионы, и от их концентрации. Вторые обусловлены структурой самого зерна ионита, его проницаемости для ионов, поглощаемых из растворов и вытесняемых в результате обмена из смеси. [3]
Процесс установления ионообменного равновесия протекает во времени. Поэтому, как правило, разделение смесей осуществляется в неравновесном режиме. Особенно это характерно для динамических методов использования ионного обмена. [4]
 |
Зависимость степени десульфирования катионита КУ-2 от продолжительности нагревания на воздухе при температурах 175 ( а, 200 ( б и 225 ( в. [5] |
Скорость установления ионообменного равновесия при титровании катионита после термообработки резко уменьшалась с увеличением СПС. [6]
Скорость установления ионообменного равновесия зависит от скорости диффузии иоиов внутрь зерен смолы, размера зерен, степени сшивки смолы, кон цеитрации ионов в растворе и других факторов. [7]
Процесс установления ионообменного равновесия начинается при помещении ионита, насыщенного соответствующим ионом, в раствор электролита. При перемешивании раствора обмен ионами идет до наступления равновесного состояния. Равновесное состояние характеризуется завершением прохождения реакции в одном направлении и зависит от концентрации обоих видов ионов, их заряда и химической и физической природы ионита. На процесс установления равновесия влияет величина рН и в меньшей степени некоторые другие факторы. [8]
Значительная скорость установления ионообменного равновесия в подобных ионитах делает их весьма перспективными сорбентами. [9]
Реакция идет до установления ионообменного равновесия. Скорость установления равновесия зависит от Внешних и внутренних факторов: гидродинамического режима жидкости; концентрации обменивающихся ионов; структуры зерен ионита, его проницаемости для ионов. Имеются разные точки зрения а механизм конного обмена. [10]
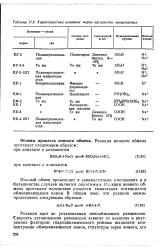 |
Характеристика основных марок катионитов, выпускаемых. [11] |
Реакция идет до установления ионообменного равновесия. [12]
Какие процессы определяют скорость установления ионообменного равновесия. Какие условия способствуют более быстрому протеканию ионного обмена. [13]
Определяющее влияние на скорость установления ионообменного равновесия, помимо степени диссоциации активных групп [4], имеет пространственная структура подвижной сетки смолы. Изменения последней, по нашему мнению, должны отражаться на плотности и набухаемости катионита. Поэтому представляет интерес изучить влияние термической обработки на плотность гидратированной и безводной смолы, а также на ее набухаемость. До настоящего времени поставлены только опыты высокотемпературной обработки смол КУ-1 и КУ-2 ( 184), при которой можно рассчитывать на значительные изменения указанных свойств катионитов. [14]
 |
Зависимость разрушающего напряжения набухших в воде мембран Анкалит К-2 ( /, МПФС ( 2, МКРП ( 3 и PAtK-101 ( 4 от температуры измерения. [15] |
Страницы: 1 2 3 4