Установление - ионообменное равновесие
Cтраница 3
Полученные минерально-органические ионообменники имели емкость 1 - 2 мэкв / г и обладали рядом достоинств, к числу которых следует отнести большую скорость установления ионообменного равновесия, ненабухаемость в водных растворах, высокую термическую и радиационную стойкость. Полученные материалы могут работать и как фильтры, задерживающие, в частности, частицы коллоидных размеров. Одним из основных недостатков этих материалов является то, что они не выдерживают кислотно-щелочной регенерации. [31]
Как уже отмечалось ранее, тепловой эффект при ионообменных процессах в общем незначителен из-за происходящих глубоких компенсаций энергии, соответственно этому также незначительно влияние температуры на установление ионообменного равновесия. [32]
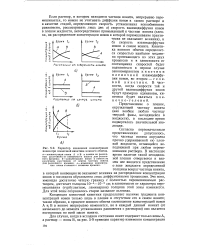 |
Характер изменения концентрации ионов при пленочной кинетике ионного обмена. [33] |
Если раствор, в котором находится частица ионита, непрерывно перемешивается, то можно не учитывать диффузии ионов в самом растворе и в качестве стадий, определяющих скорость установления ионообменного равновесия, рассматривать лишь две: а) скорость взаимодиффузии ионов в пленке жидкости, непосредственно примыкающей к частице ионита ( пленка, на распределение концентрации ионов в которой перемешивание практически не оказывает влияния), и б) скорость взаимодиффузии ионов в самом ионите. Кинетика ионного обмена определяется скоростью наиболее медленно протекающего из этих двух процессов и в зависимости от соотношения скоростей будет подчиниться в первом случае закономерностям кинетики пленочной взаимодиффузии ионов, во втором - г е л е-вой кинетике. В частности, когда скорости той и другой взаимодиффузии ионов будут примерно одинаковы, кинетика будет являться п л е-ночно-гелевой. [34]
Как уже было указано выше, феноло-формальдегидные смолы не нашли практического применения в качестве ионообменных сорбентов, так как они обладают малой степенью ионизации ионогенных групп и низкой скоростью установления ионообменного равновесия. [35]
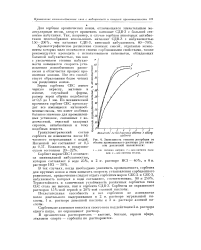 |
Зависимость степени десорбции от объема промывающего раствора для катионов различной валентности. [36] |
Хроматографическое разделение сложных смесей, отдельные компоненты которых мало отличаются своими сорбционными свойствами, также рекомендуется проводить с использованием катионитов, обладающих большой набухаемостью, так как с увеличением степени пабухае-мости повышается скорость установления ионообменного равновесия и облегчается процесс проявления колонн. Все это способствует образованию более четких зон разделения ионов. [37]
Поглощение ионов из р-ра сопровождается строго эквивалентным вытеснением подвижных ионов И. Скорость установления ионообменного равновесия определяется степенью ионизации И. [38]
Иногда реакция обмена протекает так медленно, что истинное равновесие практически не наступает. Скорость установления ионообменного равновесия зависит от многочисленных факторов, в том числе свойств ионообменника и растворителя. [39]
Поглощение ионов иа р-ра сопровождается строго эквивалентным вытеснением подвижных ионов И. Скорость установления ионообменного равновесия определяется степенью ионизации И. [40]
При этом объем регенерированной кислоты равен объему исходного раствора. Время установления ионообменного равновесия на стадии сорбции и десорбции в указанных условиях не превышает 10 минут. [41]
А и агрегатов глобул размером до 3000 А, что способствует уширению пор и большей скорости ионообмена. Наименьшая скорость установления ионообменного равновесия для пириДиниевого ионита объясняется дополнительной экстракцией золь-фракции при синтезе. [42]
Они имеют высокую скорость установления ионообменного равновесия благодаря отсутствию диффузии внутрь зерна и доступности функциональных групп. Значительно облегчена их регенерация. Высокая скорость процессов сорбции и регенерации на минерально-органических сорбентах позволяет значительно увеличивать скорости потоков растворов, протекающих через колонку. [43]
Приведенные данные справедливы для ионного обмена с участием синтетических ПАВ, находящихся в растворе в ионно-молеку-лярном состоянии. В случае достижения ККМ время установления ионообменного равновесия увеличивается в несколько раз. Данное явление можно объяснить тем, что требуется некоторое время для разрушения мицелл ПАВ и перехода их в ионы и молекулы, в виде которых синтетические ПАВ сорбируются ионитом. [44]
Полученные препараты обладают важным преимуществом перед существующими органическими ионообменными смолами: большой скоростью установления ионообменного равновесия, особенно при малых концентрациях ионов в растворах. В качестве примера на рис. 2 сопоставлены кривые установления ионообменного равновесия в растворе NaCl концентрации 2 10 N для ионита КУ-2 и для полученного нами ионообменника на основе белой сажи и полистирола с последующим сульфированием. Как следует из рисунка, в нашем случае скорость установления равновесия значительно выше. Интересно также отметить, что на минерально-органических ионообменных материалах скорость установления ионообменного равновесия не лимитируется внутренней, так называемой голевой, диффузией ионов, как это имеет место в случае обычных ионообменных смол. Стрелкой указан момент извлечения сорбента из раствора на 12 час. [45]
Страницы: 1 2 3 4