Устойчивость - аммиакат
Cтраница 2
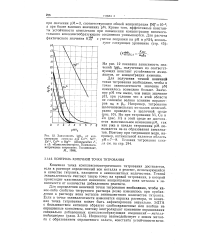 |
Зависимость IgpA от концентрации аммиака для Со2, № 2, Zn2, Cu2 и Hg2 ( Шварценбах Г., в сб. Комплексометрия, Комплексо-метрическое титрование, Госхимиздат, М., 1968. [16] |
На рис. 12 показана зависимость значений g A, полученных из соответствующих констант устойчивости аммиакатов, от концентрации аммиака. [17]
 |
Электродные потенциалы для металлов в жидком аммиаке при 25 С. [18] |
Но если используются достаточно чистые реагенты, то при низкой температуре скорость разложения очень мала, причем устойчивость аммиакатов разных элементов различна. [19]
Резкое увеличение энергии поляризации в ряду галогенидов от хлора к иоду может привести к полному обращению рассматриваемых рядов устойчивости аммиакатов. [20]
В случае же солей с сильно выраженной взаимной поляризацией ионов ( точнее, с химической связью, приближающейся по типу к ковалентной связи) наблюдаются обратные соотношения - устойчивость аммиакатов уменьшается в ряду хлорид, бромид, иодид. [21]
Однако в тех случаях, когда возможно образование кова-лентной связи между центральным ионом и анионом, находящимся во внешней сфере, общая картина изменения устойчивости нарушается - наряду с нормальными рядами устойчивости аммиакатов наблюдаются также полностью или частично обращенные ряды. [22]
Количественной характеристикой устойчивости комплексных ионов могут служить значения их констант нестойкости, или констант устойчивости, применение которых облегчает рассмотрение способности элементов к комплексообразованию в зависимости от порядкового номера элемента. Например, устойчивость аммиакатов и способность к комплексообразованию от Соа к Си2 повышается, а затем при переходе к Zn2 падает. [23]
Кривые, выражающие границы этих областей устойчивости как функции температуры, могут пересекаться. Соотношения, определяющие устойчивость гидратированных аммиакатов, напри-мер Cu ( NH3) 4S04 - H20, более сложны. [24]
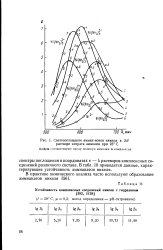 |
Светопоглощение аммин-ионов никеля в 2N растворе нитрата аммония при 23 С. [25] |
В табл. 10 приводятся данные, характеризующие устойчивость аммиакатов никеля. [26]
На устойчивость аммиакатов солей с одним и тем же центральным ионом существенное влияние оказывают величина и заряд анионов, находящихся во внешней сфере. При учете одних только электростатических сил можно было бы сделать вывод о том, что с уменьшением заряда и увеличением размера внешних анионов устойчивость комплексных аммиакатов должна возрастать. Подобные ряды устойчивости аммиакатов действительно наблюдаются в случае галогенидов некоторых металлов и известны под названием нормальных рядов устойчивости. [27]
Способность к комплексообразованию зависит от природы применяемого амина. Легче всего получаются и являются наиболее устойчивыми комплексы с 1 2-диаминами, в частности, с этиленди-амином и пропилендиаминрм. Особая устойчивость производных этилендиамина ( превосходящая устойчивость аммиакатов) впоследствии станет понятной в связи с рассмотрением вопроса об устойчивости комплексных соединений, содержащих пяти - и шестичлен-ные циклы. [28]
Способность к комплексообразованию зависит от природы применяемого амина. Легче всего получаются и являются наиболее устойчивыми комплексы с 1 2-дпаминами, в частности, с этиленди-амином и пропилендиамином. Особая устойчивость производных этилендиамина ( превосходящая устойчивость аммиакатов) впоследствии станет понятной в связи с рассмотрением вопроса об устойчивости комплексных соединений, содержащих пяти - и шестичлен-ные циклы. [29]
Они постоянны, только если постоянна эта концентрация. В аналитической химии часто пользуются зависимостью реальной константы Кг от концентрации [ S3I для выяснения влияния побочного равновесия на главное равновесие. Например, если главным выступает равновесие образования аммиакатов, а побочным - равновесие протонирования молекул аммиака, зависимость / С от концентрации ионов водорода ( вещество S3) или от рН показывает влияние кислотности среды на устойчивость аммиакатов. [30]
Страницы: 1 2 3