Устойчивость - золе
Cтраница 1
Устойчивость золя определяется наличем у его частиц электрического заряда и сольватной оболочки. Частицы, не имеющие соль-ватной оболочки и электрического заряда, неустойчивы и быстро коагулируют. [1]
Устойчивость золя можно нарушить, устранив одноименный заряд коллоидных частиц и защитную гид-ратную оболочку. [2]
Устойчивость золя определяется рН среды, концентрацией SiC2 и органических растворителей. Полярные растворители ( спирт) стабилизируют поликремниевую кислоту, так как образуются комплексы на основе водородных связей. [3]
Устойчивость золя зависит от электрического заряда его дисперсной фазы. Если золь иодида серебра приготовляется из нитрата серебра прибавлением к нему в избытке иодида калия, то частицы иодида серебра остаются коллоидными потому, что они способны адсорбировать Л - - ионы. В результате такой адсорбции поверхность частиц AgJ становится отрицательно заряженной. Вокруг этих частиц распределяется эквивалентное количество положительных ионов, так что весь раствор в целом остается электронейтральным. Так образуется диффузионный двойной электрический слой, свойства которого определяют стабильность этой системы. [4]
Устойчивость золя понижается, что может привести к его коагуляции и выпадению белковой фазы в осадок. [5]
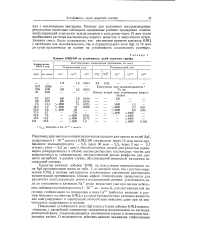 |
Влияние КМЦ-300 на устойчивость золей йодистого серебра. [6] |
Повышение устойчивости золя Agl в присутствии добавок КМЦ связано, очевидно, с адсорбцией одноименно заряженных макроанионов на частицах дисперсной фазы, сопровождающейся увеличением заряда и потенциала коллоидных частиц. [7]
Самопроизвольное понижение устойчивости золя очень сильно зависит от условий, в которых хранится золь. Например, стабильность золя сульфида р тути сравнительно быстро понижается при хранении в открытом сосуде, что объясняется улетучиванием из раствора сероводорода, являющегося стабилизатором свежеприготовленного золя сульфида ртути. При хранении золя сульфида ртути в заполненном доверху герметически закрытом сосуде золь не только не коагулирует, но становится при хранении даже более устойчивым к действию электролитов. [8]
Таким образом, устойчивость золя SiO2 является экстремальной функцией рН с минимумом, лежащим в интервале рН Зч-6. Например, высокозаряженный золь кварца при рН 6 ведет себя как типичный ионостабили-зированный коллоид, чувствительный к добавлению небольших количеств электролита. В то же время при рН 2 ( область изоэлектрического состояния), а также при рН, равных 9 и 11, он становится практически ионоиндифферентным. [9]
Строго говоря, устойчивость золя обусловлена не столько собственным движением коллоидных частиц ( или их перемещениями под действием ударов молекул среды), сколько постоянным самоперемешиванием системы, происходящим в результате практически неизбежных небольших местных изменений ее температуры. Следовательно, между коллоидными растворами и взвесями не только нет, но и не может быть четкой границы. [10]
Строго говоря, устойчивость золя обусловлена не столько собственным движением коллоидных частиц ( или их перемещениями под действием ударов молекул среды), сколько постоянным самоперемешиванием системы, происходящим в результате практически неизбежных небольших местных изменений ее температуры. Следовательно, между коллоидными растворами и взвесями не только нет, но и не может быть четкой границы. [11]
Интересно, что устойчивость золя иодида серебра с отрицательно заряженными частицами несколько выше, чем с положительно заряженными. [12]
 |
Влияние длины цепи КМЦ на устойчивость золей йодистого серебра. [13] |
Разумеется, повышение устойчивости золя в присутствии солей КМЦ, связанное с его превращением из гидрофобного в гидрофильный, не должно зависеть от знака заряда коллоидных частиц. Это подтверждается результатами опытов на положительном золе Agl. Флоккуляция золя в присутствии столь малых количеств сильноадсорбирующихся макромолекул ( макроанионов), практически нацело поглощающихся дисперсной фазой, происходит по нейтрализационному механизму - в результате снижения заряда и потенциала коллоидных частиц. [14]
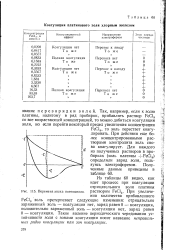 |
Коагуляция платинового золя хлорным железом.| Перемена знака потенциала. [15] |
Страницы: 1 2 3 4