Устойчивость - золе
Cтраница 3
Явление повышения порогов коагуляции ( увеличение устойчивости золя) при добавлении ВМВ называют коллоидной защитой. [31]
 |
Влияние концентрации дисперсной фазы на устойчивость золей Agl, содержащих добавки КМЦ-300. [32] |
Дальнейшее прибавление полиэлектролита сначала вызывает нарушение устойчивости золя, но, начиная с определенной концентрации КМЦ в растворе - тем меньшей, чем выше молекулярный вес полимера - устойчивость системы резко возрастает. Как показывают злектрофоретиче-ские измерения, это увеличение стабильности связано с перезарядкой коллоидных частиц; в результате адсорбции макроанионов золь из положительного превращается в отрицательный. О перезарядке частиц свидетельствует и тот факт, что защищенный становится чувствительным к катионам, причем устойчивость его к добавкам неорганических электролитов чрезвычайно возрастает. В этом отношении положительный золь Agl, содержащий 1 х X 1 ( П4 мг моль 1л КМЦ-300 и К. МЦ-500, повторяет свойства отрицательно заряженного коллоидного раствора. Все эти факты подтверждают высказанную точку зрения о доминирующей роли гидрофилиза-ции дисперсной фазы в стабилизации коллоидного раствора в присутствии КМЦ. [33]
Его присутствие может служить причиной понижения устойчивости золя, поэтому одним получением золя по той или иной реакции не заканчивается приготовление коллоидной системы: ее необходимо освободить от электролитов. Это осуществляется различными путями, наиболее важные из которых мы опишем. [34]
В остальной области рН и концентраций металла устойчивость золя высока и возрастает по мере приближения рН к нейтральным значениям и снижения концентрации металла в растворе. Обобщая проведенные расчеты, можно отметить положения, приведенные ниже. [35]
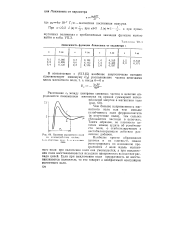 |
Зависимость функции Ланжевена от параметра е.| Влияние магнитного поля. [36] |
Чем больше напряженность магнитного поля или чем меньше устойчивость золя ферромагнетита ( в отсутствие поля), тем сильнее сближаются частицы в цепочках. [37]
Деформируемость частиц; чем легче деформируются частицы, тем выше устойчивость золя при одинаковых ПАВ, температуре и других параметрах. Это связано с тем, что способность частиц деформироваться при сближении позволяет реализовать энергетически более выгодные ( близкие к плоским) жидкие прослойки. [38]
Спирт, введенный вместе с канифолью как растворитель, отрицательно влияет на устойчивость золя. Поэтому, если золь необходимо сохранять длительное время, спирт нужно удалить диализом. [39]
Из этого правила найдены исключения, когда падение - потенциала сопровождается возрастанием устойчивости золя, а возрастание - потенциала сопровождается коагуляцией. [40]
Внешние фактор воздействия на гидрозоль неорганического коллоида могут в большой степени повлиять на устойчивость золя. Это снижает роль гидратных оболочек: они те-перь уже в меньшей степени экранируют ( заслоняют) частицы о: действия молекулярных сил сцепления. Коллоидные частицы, совершая броуновское движение, могут при столкновении приближаться настолько, что между ними начинают проявлять себя силы Ван-дер - Ваальса. В результате мицеллы начинают слипаться, частицы дисперсной фазы укрупняются. В результате этого коллоидный раствор как таковой перестает существовать-он разрушается. Иногда первую стадию процесса ( слипание первичных коллоидных частиц в агрегаты) обозначают как скрытую коагуляцию, а вторую стадию ( образование крупных хлопьев и их осаждение - как явную коагуляцию. [41]
 |
Схема строения коллоидной частицы ( мицеллы гидроксида железа ( III. [42] |
Внешние факторы воздействия на гидрозоль неорганического коллоида могут в большой степени повлиять на устойчивость золя. Это снижает роль гидратных оболочек: они теперь уже в меньшей степени экранируют ( заслоняют) частицы от действия молекулярных сил сцепления. Коллоидные частицы, совершая броуновское движение, могут при столкновении приближаться настолько, что между ними начинают проявлять себя силы Ван-дер - Ваальса. В результате мицеллы начинают слипаться, частицы дисперсной фазы укрупняются. [43]
Видно, что при рН 3, как и при рН 6 наблюдается скачкообразное изменение устойчивости золя, однако полной стабилизации системы не происходит. Расчет энергии взаимодействия частиц SiO2 по теории ДЛФО показывает, что наблюдаемая агрегация связана с первичным минимумом на кривой энергии взаимодействия частиц. Наличие структурной составляющей энергии взаимодействия, возникающей при перекрытии ГС воды, а также, возможно, адсорбционных слоев ЦТАБ на кварце, препятствует непосредственному сближению частиц и достижению высоких степеней агрегации. [44]
При прибавлении защитного коллоида в количестве, недостаточном для защиты, может происходить не повышение устойчивости золя, а понижение ее. [45]
Страницы: 1 2 3 4