Устойчивость - золе
Cтраница 2
Такое явление периодического чередования устойчивости золя с зонами коагуляции носит название неправильных рядов коагуляции или зон коагуляции. [16]
Защита проявляется в повышении устойчивости лиофобного золя при прибавлении к нему раствора высокомолекулярного вещества. [17]
Стабилизаторами называются вещества, обусловливающие устойчивость золя. Стабилизаторами могут быть как реагенты, из которых получился золь, так и посторонние примеси, ионы или молекулы которых могут адсорбироваться на поверхности частиц и придавать им устойчивость. [18]
Если это так, то устойчивость золя должна быть следствием стерической стабилизации, вызванной образованием водородных связей между силанольными группами поверхности кремнезема и атомами кислорода эфирных и гид-роксильных групп органического вещества. [19]
Это вызывает появление второй зоны устойчивости золя. Еще большее увеличение содержания электролита в дисперсной среде приводит к сжатию диффузных частей двойных электрических слоев, что снова уменьшает значение электрокинетического потенциала и вместе с тем приводит к снижению устойчивости золя. [20]
Под привыканием обычно подразумевается увеличение устойчивости коагулируемого золя в зависимости от способа прибавления электролита при коагуляции. Установлено, что количество необходимого для коагуляции вещества различно, в зависимости от того, прибавлялся ли электролит сразу или постепенно небольшими порциями - в последнем случае обычно приходится прибавлять гораздо - больше электролита, чтобы вызвать такое же явление коагуляции. [21]
Когда потенциал ф0 частиц невысок, устойчивость золя зависит от значения пт § нди. Для объяснения коагуляции золя с сильно заряженными частицами теория ДЛФО исходит уже из рредставлений о сжатии двойного электрического слоя, согласно которым объясняется правило Шульце - Гарди. Существенно, что оба правила приложимы к золям одной и той же природы, а иногда и при одинаковом составе электролита. [22]
Когда потенциал ро частиц невысок, устойчивость золя зависит от значения потенциала-поверхности, а адсорбционные явления определяют коагуляционный процесс; этим, как мы видели, объясняется правило Эйлерса - Корфа. Для объяснения коагуляции золя с сильно заряженными частицами теория ДЛФО исходит уже из представлений о сжатии двойного электрического слоя, согласно которым объясняется правило Шульце-Гарди. Существенно, что оба правила приложимы к золям одной и той же природы, а иногда и пр и одинаковом составе электролита. [23]
Второй род сил, влияющих на устойчивость золя - силы притяжения между частицами. Они имеют ту же природу, что и силы, действующие между нейтральными молекулами. [24]
Когда потенциал ро частиц невысок, устойчивость золя зависит от значения потенциала-поверхности, а адсорбционные явления определяют коагуляционный процесс; этим, как мы видели, объясняется правило Эйлерса - Корфа. Для объяснения коагуляции золя с сильно заряженными частицами теория ДЛФО исходит уже из представлений о сжатии двойного электрического слоя, согласно которым объясняется правило Шульце-Гарди. Существенно, что оба правила приложимы к золям одной и той же природы, а иногда и пр и одинаковом составе электролита. [25]
Второй род сил, влияющих на устойчивость золя, - силы притяжения между частицами. Они имеют ту же природу, что и силы, действующие между нейтральными молекулами. [26]
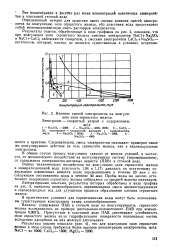 |
Влияние смесей электролитов на коагуляцию золя сернистого железа. Электролит - хлористый натрий с содержанием. [27] |
Присутствие в пластовой воде ПАВ увеличивает устойчивость золя сернистого железа из-за гидрофилизации поверхности коллоидных частиц вследствие адсорбции на них молекул диссольвана. [28]
Увеличение порога коагуляции является результатом повышения устойчивости золя. [29]
 |
Зависимость оптической плотности А золя от объема добавленного электролита. [30] |
Страницы: 1 2 3 4