Устойчивость - анион
Cтраница 1
Устойчивость тритильного аниона повышается при замещении в нем водородов в пара-положении на группы с большим - С-эффек-том. Три ( - нитрофенил) метилкалий устойчив в спиртовых растворах и, следовательно, его рКа меньше, чем этилового спирта. [1]
Устойчивостью триарилметильного аниона объясняется подвижность ( легкое отщепление в виде протона) метанового водорода три-арилметанов, а устойчивостью триарилметильного катиона - подвижность хлора в триарилхлорметанах. [2]
Устойчивостью триарилметильного аниона объясняется подвижность ( легкая протонизируемость) метанового водорода триарилметанов, а устойчивостью триарильного аниона - подвижность хлора в триарилхлор-метанах. [3]
Объяснение устойчивости аниона было впервые дано Хюккелем: электронный секстет заполняют, как и в бензоле, три связывающие орбитали, все разрыхляющие орбитали свободны. Сейчас он известен как ион тропилия, образующий солеподобные соединения, например C-H Bf. Синтез иона тропилия и исследование его свойств были триумфом теории Хюккеля. Имея соответственно 4 и 8 я-электро-нов, эти молекулы не подчиняются правилу ( 4и 2) Хюккеля. [4]
Очевидно, устойчивость аниона является главной движущей силой его образования. [5]
В том же ряду устойчивость анионов возрастает, так как при переходе от С1О - к СЮг увеличивается число электронов, принимающих участие в образовании связей атомов С1 и О. При этом порядок связи возрастает от 1 до 1 5, что проявляется в увеличении энергии связи от 209 до 363 5 кДж / моль. В связи с этим в приведенном ряду окислительная активность анионов уменьшается. Если гипо-хлориты проявляют окислительные свойства в любой среде, а хлораты - только в сильнокислой, то перхлораты практически не являются окислителями. [6]
В том же ряду устойчивость анионов возрастает, так как при переходе от СЮ к СЮ4 увеличивается число электронов, принимающих участие в образовании связей атомов С1 и О. При этом порядок связи возрастает от 1 до 1 5, что проявляется в увеличении энергии связи от 209 до 363 5 кДж / моль. В связи с этим в приведенном ряду окислительная активность анионов уменьшается. Если гипохлориты проявляют окислительные свойства в любой среде, а хлораты - только в сильнокислой, то перхлораты практически не являются окислителями. [7]
При уменьшении радиуса катиона устойчивость аквокомплек-са аниона фтора снижается, и фториды лития и натрия не образуют кристаллогидратов; возможность образования аквокатионов в этих солях исключается малым радиусом ионов фтора, прочие галогениды тех же металлов образуют кристаллогидраты, в которых вода связана с катионами. [8]
Устойчивость калиевой соли бъясняется устойчивостью аниона флуорена. [9]
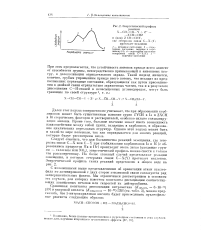 |
Энергетический профиль. [10] |
При этом предполагается, что устойчивость анионов прежде всего зависит от способности группы, непосредственно примыкающей к анионному центру, к делокализации отрицательного заряда. [11]
Отсюда был сделан вывод, что устойчивость алкильных анионов убывает в ряду RCH - R2CH - R3C -, т.е. в порядке, обратном изменению устойчивости алкильных катионов. Так, в то время как метиллитий ( и фениллитий) устойчивы в эфирном растворе, / ирети-бутиллитий быстро разлагает эфир. [12]
Отсюда был сделан вывод, что устойчивость алкильных анионов убывает в ряду RCHa - R2CH - R3C -, т.е. в порядке, обратном изменению устойчивости алкильных катионов. Так, в то время как метиллитий ( и фениллитий) устойчивы в эфирном растворе, тгерет-бутиллитий быстро разлагает эфир. [13]
Необходимое для отчетливого проявления окислительных свойств уменьшение устойчивости аниона может быть достигнуто также при помощи нагревания. [14]
Скорость изомеризации зависит от активности катализатора; увеличивающего устойчивость отщепляющегося аниона. [15]
Страницы: 1 2 3