Устойчивость - комплекс
Cтраница 1
 |
Константы нестойкости некоторых комплексных ионов в водном растворе при 25 С. [1] |
Устойчивость комплексов часто характеризуют обратной величиной 1 / К - Э, называемой константой устойчивости комплекса. [2]
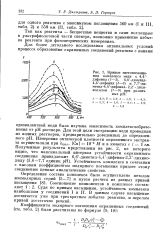 |
Кривые светопоглоще-ния комплекса меди с 4 4 -дифенил ( 1 - 3, 6 6 -диметил - 4 4 -дифенил ( 4 - б п 7 7 -ди-метил - 4 4 -дифенил - 2 2 - дихи-нолилом ( 7 - 9 при различных рН. [3] |
Устойчивость комплекса в сочетании с высоким коэффициентом молярного погашения придает этому соединению ценные аналитические свойства. [4]
Устойчивость комплекса зависит также от основности хелати-рующего агента. Под термином хелатирующий агент подразумевают анион, с которым фактически взаимодействует металл, а не неионизированную молекулу лиганда. Это обобщение подтверждается результатами, полученными Калвином и Вильсоном [158] на примере комплексов замещенных салицилового альдегида, а также Калвином и Байлсом [159] в случае комплексов замещенных салицилальиминов. [5]
Устойчивость комплекса существенно зависит от рН раствора. Поэтому комплексонометрическое титрование ведут в заданном интервале рН, используя различные буферные растворы. [6]
Устойчивость комплексов удобно характеризовать значениями констант их диссоциации ( см. гл. [7]
Устойчивость комплексов характеризуется константой диссоциации ( нестойкости) Кобщ, или константой образования. Диссоциация координационной сферы происходит ступенчато. Каждая стадия диссоциации комплекса определяется ступенчатой константой диссоциации Ki, Kz Кп-Чем больше значение / Сдис, тем менее устойчива комплексная частичка. Для разрушения комплексного соединения необходимо связать одну из частичек, образующихся при диссоциации комплекса, в менее диссоциированное соединение, что приводит к смещению равновесия в сторону диссоциации комплекса. [8]
Устойчивость комплексов [ М ( Н2О) 6 ] 2, как и других комплексов со слабыми лигандами, например [ MFe ] 4 -, возрастает по мере заполнения электронами - уровня. Первый максимум на кривой констант нестойкости достигается у иона ванадия [ V ( H2O) 6 ] 2 i, что выражается в минимальном значении константы нестойкости этого иона. При переходе к иону [ Мп ( Н2О) б ] 2 константы нестойкости повышаются, что отвечает заполнению уровней tig и ее неспаренными электронами. Далее максимум устойчивости и минимум констант нестойкости приходится на ион [ № ( Н2О) б ] 2, у которого g - уровень заполнен спаренными электронами, а уровень ее содержит только неспаренные электроны. При дальнейшем заполнении уровня центрального атома электронами константы нестойкости возрастают. [9]
Устойчивость комплекса зависит также и от соотношения радиусов ( объемов) комплексообразователя и лигандов. [10]
 |
Константы нестойкости некоторых комплексных ионов в водном растворе при 23 С. [11] |
Устойчивость комплексов часто характеризуют обратной величиной 1 / / Г - Э, называемой константой устойчивости комплекса. [12]
Устойчивость комплексов в растворах слабо зависит от температуры. [13]
 |
Параметры катионов металла ам и 6М для 25 С. [14] |
Устойчивость комплексов растет с ростом заряда и уменьшением радиуса катиона. [15]
Страницы: 1 2 3 4