Устойчивость - комплекс
Cтраница 3
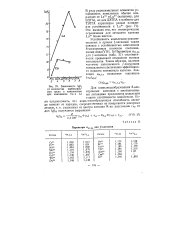 |
Зависимость Igpi от количества карбоксильных групп в комплексоне Вля комплексов Са и La. [31] |
Устойчивость комплексов редкоземельных и прочих f - катионов также связана с устойчивостью комплексов 8-электронных катионов соотношениями вида ( VIII. Параметры j3M La для / - катионов ( табл. 31) систематически превышают отношение ионных потенциалов. Таким образом, наличие частично заполненного / - подуровня эквивалентно увеличению эффективного ионного потенциала катиона. [32]
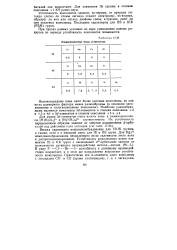 |
Координационные числа ( / - элементов. [33] |
Устойчивость комплексов зависит, во-первых, от природы ли-ганда ( легко ли атомы лиганда отдают электроны), во-вторых, образует ли ион или лиганд двойные связи, в-третьих, дают ли они хелатные комплексы. Последние характерны для ПБ и ШБ ( РЗМ) групп. [34]
Устойчивость комплекса обеспечивается двумя пятичленными циклическими группировками. В настоящее время установлено, что в этом соединении, кроме двух пятичленных циклов, образованных оксимными атомами азота и ионом никеля, имеются два дополнительных шестичленных цикла, образованных посредством водородных связей. [35]
Устойчивость комплексов [ Ре ( СО) 4 ( г1: г-оле-фин) ] повышается с ростом электроноакцепторных св-в олефина. При действии на них НС1 н НВг расщепляется я-связь Ре-олефин с образованием алканов. Амины, фосфн-ны и др. доноры электронной пары замещают СО или олефин. Для катионных комплексов характерны р-ции с нуклеофилами, напр. [36]
Устойчивость комплексов определяется природой центр, атома и лиганда и стерич. Льюиса и мягкие к-ты Льюиса. Первые имеют малый атомный или ионный радиус и высокую положит, степень окисления, предпочтительно взаимод. К-ты второго класса имеют большой атомный или ионный радиус и низкую степень окисления, более эффективно взаимод. Мягкие к-ты Льюиса имеют электроны на ( / - орбиталях, способные к образованию л-связей в результате перекрывания с вакантными с / - орби-талями мягких лигандов. [37]
Устойчивость комплексов меняется от весьма стабильных соед. И) до комплексов А § ( 1) или Си ( 1), существование к-рых в р-рах доказано косвенными методами. Она возрастает для комплексов металлов в низкой или нулевой степени окисления при наличии электроноакцепторных заместителей при двойной связи, напр. [38]
Устойчивость комплексов некоторых металлов с а-окси-а-пиридилметан - сульфоновыми кислотами. [39]
Устойчивость комплексов обычно сильно возрастает при хелатировании металла. [40]
Устойчивость комплексов, образуемых ЭДТА и ее солями, настолько высока, а концентрация свободного катиона, образованного диссоциацией комплексона, так мала, что при этом не может быть достигнута величина произведения растворимости для всех труднорастворимых соединений, обычно присутствующих в воде тепловых электростанций. Это означает, что при нормальной температуре все примеси ( и естественные и продукты коррозии) будут находиться в воде только в растворенном состоянии. [41]
Устойчивость комплекса определяется величиной константы равновесия его образования. На языке термодинамики константа равновесия реакции является мерой выделившейся в реакции теплоты и изменения энтропии при реакции. Большее количество выделившейся теплоты приводит к образованию более устойчивых продуктов реакции. Энтропия системы является мерой беспорядка; больший беспорядок относительно исходных веществ, обусловленный образованием продуктов реакции, приводит к увеличению энтропии при реакции и к большей устойчивости конечных продуктов. [42]
Устойчивость комплекса катализатор-субстрат определяется не только природой центрального иона, ее можно также регулировать в широких пределах при введении в координационную сферу металла различных лигандов. Например, лиганды CN -, PPhg, СО, SnClg и др., обладающие электроноакцепторными свойствами, способствуют окислению катализатора, что приводит к координированию субстрата. Лиганды такого типа чаще всего служат активаторами в рассматриваемых процессах. При этом лиганды, способствующие чрезмерному упрочнению связи катализатор-субстрат, вместо ускорения реакции могут вызывать ее замедление. Так, в реакциях гидрирования алкенов и ал-кинов наибольшей каталитической активностью обладают комплексы иридия 1гН ( СО) ( РРЬз) з и транс - 1гС1 ( СО) ( РРЬз) 2, которые удерживают водород не очень прочно, тогда как комплекс иридия Ir ( Ph2PCH2CH2PPh2) X, присоединяющий водород необратимо, каталитически неактивен. В той же последовательности возрастает и способность комплексов к образованию умеренно прочных гидридов. [43]
Устойчивость комплекса возрастает с повышением радиуса иона щелочного металла и с уменьшением величины алкильного остатка. В связи с этим представляют интерес систематические исследования комплексных соединений высших алюминийал-килов. [44]
Устойчивость комплексов такого типа тем больше, чем больше электроноотталкивающих групп ( например, групп СН3 и других заместителей первого рода), увеличивающих электронную плотность в ядре, содержит бензоидная компонента и чем большим числом электронопритягивающих заместителей обладает хиноидная компонента. [45]
Страницы: 1 2 3 4